Trong bảng tuần hoàn các nguyên tố hóa học, kim loại kiềm thuộc nhóm
A. IA.
B. IIIA.
C. IVA.
D. IIA.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.
Trong bảng tuần hoàn các nguyên tố hóa học, kim loại kiềm thuộc nhóm
A. IA.
B. IIIA.
C. IVA.
D. IIA.


Theo đề bài ta có : 2Z + N = 40
N ≥ Z . Vì vậy ta có : 3Z ≥ 40, do đó Z ≤ 40/3 = 13,3 (1)
Măt khác : N/Z ≤ 1,5 → N ≤ 1,5Z
Từ đó ta có : 2Z + N ≤ 2Z + 1,5Z; 40 ≤ 3,5Z
→ Z ≥ 40/3,5 = 11,4 (2)
Tổ hợp (1) và (2) ta có : 11,4 ≤ Z ≤ 13,3 mà z nguyên. Vậy Z= 12 và Z = 13.
Nếu Z = 12 thì N = 16 và A = 28 (trái với đề bài A < 28)
Vậy Z = 13. Đó là nguyên tố nhôm (Al).
Vị trí của nhôm trong bảng tuần hoàn :
+ Ô số 13 ;
+ Chu kì 3 ;
+ Nhóm IIIA.

Đáp án A.
Ta xét hai trường hợp sau:
- Nếu X và Y thuộc chu kì nhỏ thì ta có
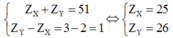
(loại do nhóm IIA và IIIA)
Nếu X và Y thuộc chu kì lớn thì ta có
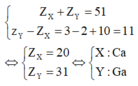
Nhận xét các đáp án:
A đúng: Ca không khử được ion Cu2+ trong dung dịch vì khi cho Ca vào dung dịch chứa Cu2+ thì Ca phản ứng với H2O có trong dung dịch trước:
![]()
Sau đó Cu2+ sẽ phản ứng với OH-:
![]()
B sai: Ở nhiệt độ thường Ca khử được H2O:
![]()
C sai: Hợp chất của Ca với oxi là CaO
D sai: Trong nguyên tử Ca có 20 proton

Chọn B
![]()
X và Y thuộc cùng một chu kì và hai nhóm liên tiếp (nhóm IIA và IIIA) nên ta có các trường hợp sau


Ở nhiệt độ thường X khử được nước, không khử được ion C u 2 + trong dung dịch (do sẽ phản ứng với nước trước), hợp chất với oxi có dạng CaO, trong X có 20 proton.

ZX +ZY =51→X,Ythuộc cùng một chu kì lớn trong bảng tuần hoàn. Khi đó, nhóm IA và IIA bị ngăn cách bởi các nguyên tố nhóm B, do đó ta có:
ZX +10+1= ZY ; ZX +ZY =51→ ZX =20 (Ca) và ZY = 31 (Ga)
A. Đúng. Trong dung dịch, Ca khử nước trước tạo thành Ca(OH)2 nên không khử được Cu2+.
B. Sai. Hợp chất với oxi của X có dạng XO (CaO).
C. Sai. Trong nguyên tử của nguyên tố X có 20 proton.
D. Sai. Ở nhiệt độ thường canxi có thể khử được nước tạo thành dung dịch Ca(OH)2 và giải phóng khí H2.
Chọn đáp án A.
Đáp án A