Nguyên tố R là phi kim thuộc nhóm A. Hợp chất của R với hiđro là R H 3 . Hóa trị với số oxi hóa của R trong oxit tương ứng với hóa trị cao nhất lần lượt là
A. 3 và -3
B. 5 và -5
C. 5 và +5
D. 3 và +3
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Oxit cao nhất của một nguyên tố R thuộc nhóm A có dạng RO3
=>Hóa trị cao nhất của R với oxi là 6 R có công thức electron lớp ngoài cùng
=>R là một phi kim.
Hóa trị với hidro là: 8 – 6 = 2
=>Công thức hợp chất khí với hidro hóa là RH2
Axit tương ứng của RO3 là H2SO4.
Các nhận định đúng là (1),(2),(3).
Đáp án C.

Chọn D
Gọi hóa trị cao nhất của R trong oxit là m, hóa trị trong hợp chất với hiđro là n. Ta có: m + n = 8.
Theo bài: m = 3n. Từ đây tìm được m = 6; n = 2.
=> Hóa trị của R trong hợp chất khí với H là 2.

Chọn B
R có 4 electron lớp ngoài cùng, e cuối cùng điền vào phân lớp np → R thuộc nhóm IVA
→ Hợp chất khí với hiđro và oxit cao nhất của R lần lượt là R O 2 , R H 4 .
Ta có:
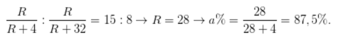

Chọn A
Gọi n là hóa trị của R trong oxit thì hóa trị của R trong hợp chất với hiđro là (8-n)
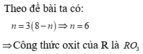

Đáp án D
R có 6e lớp ngoài cùng, hóa trị cao nhất với oxi = 6, hidro = 2.

Chọn D
Nguyên tố R có cấu hình electron lớp ngoài cùng là ns2np4 → R thuộc nhóm VIA.
→ Công thức oxit cao nhất của R là RO3; công thức hợp chất khí với H của R là RH2.
Chọn C
Hợp chất của R với hiđro là RH3 → Công thức oxit cao nhất của R là R2O5.
→ Số oxi hóa của R trong oxit cao nhất là +5.