Trong tự nhiên Cu có hai đồng vị: C 29 63 u , C 29 65 u . Khối lượng nguyên tử trung bình của Cu là 63,54. Thành phần % về khối lượng của C 29 63 u trong CuCl2 là giá trị nào dưới đây? Biết MCl = 35,5.
A. 73,00 %
B. 27,00%
C. 32,33%
D. 34,18 %
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(\%^{63}_{29}Cu=x\%\Rightarrow\%^{65}_{29}Cu=100\%-x\%\)
\(\overline{M}=\dfrac{x\%\cdot63+\left(100-x\right)\%\cdot65}{100\%}=63.54\)
\(\Rightarrow x=73\)
\(\dfrac{\%^{63}_{29}Cu}{\%^{65}_{29}Cu}=\dfrac{73}{100-73}=\dfrac{73}{27}\)

Gọi phần trăm số nguyên tử của hai đồng vị \(^{63}_{29}Cu\) và \(^{65}_{29}Cu\) lần lượt là a và b.
Ta có: \(\left\{{}\begin{matrix}a+b=100\%\\63a\%+65b\%=63,54\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}a=73\%\\b=27\%\end{matrix}\right.\)
Phần trăm khối lượng \(^{63}_{29}Cu\) trong \(Cu\left(NO_3\right)_2\) là:
\(\dfrac{63\cdot0,73}{63,54+14\cdot2+16\cdot6}\cdot100\%=24,52\%\)

73%
áp dụng công thức
gọi x là 63cu
->65cu 100-x
thê vào giải là ra

Ta có : nguyên tử khối trung bình của đồng được tính theo công thức :
63,54 = \(\frac{165+\left(100-a\right)63}{100}\)
Trong đó a là phần trăm số nguyên tử \(\frac{65}{29}Cu,q,\left(100-a\right)\) là phần trăm số nguyên tử \(\frac{63}{19}Cu\) . Giải ra ta có a = 27%
Vậy \(\frac{65}{29}Cu\) có 27% , \(\frac{63}{29}Cu\) có 73 %

Đáp án D
• Giả sử % của 63Cu, 65Cu trong tự nhiên lần lượt là x, y.
Ta có hpt:
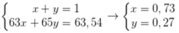
→ Phần trăm của 63Cu trong CuCl2 là
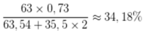

Chọn D
Gọi phần trăm đồng vị C 29 63 u = x , thì % đồng vị C 29 65 u = 100 - x ;
Ta có
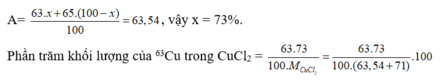
=34,18%

Chọn A
Gọi phần trăm đồng vị C 63 u = x, thì % đồng vị 6 C 65 u = 100 - x
Ta có
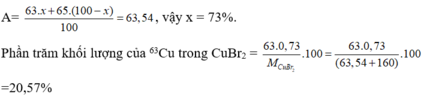
Đáp án D.
Phần trăm đồng vị 63Cu = x, thì % đồng vị 65Cu = 100 - x
Ta có: