Hòa tan hoàn toàn 5,4 gam Al trong dung dịch H2SO4 1M thu được V lít khí ( đktc ) và dung dịch X
a) Tính V?
b) Tính nồng độ mol/l của các chất tan trong X biết rằng H2SO4 dư 10% so với lượng phản ứng và thể tích dung dịch X bằng thể tích dung dịch H2SO4 ban đầu

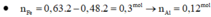
a) \(n_{Al}=\frac{5,4}{27}=0,2\left(mol\right)\)
PTHH : \(2Al+3H_2SO_4-->Al_2\left(SO_4\right)_3+3H_2\)
Theo pthh : \(n_{H_2}=\frac{3}{2}n_{Al}=0,3\left(mol\right)\)
=> \(V_{H_2}=0,3\cdot22,4=6,72\left(l\right)\)
b) Theo pthh :
\(n_{Al_2\left(SO_4\right)_3}=\frac{1}{2}n_{Al}=0,1\left(mol\right)\)
\(n_{H_2SO_4\left(pứ\right)}=\frac{3}{2}n_{Al}=0,3\left(mol\right)\) => \(V_{H_2SO_4}=\frac{\left(0,3+0,03\right)}{1}=0,33\left(l\right)\)
=> \(n_{H_2SO_4\left(dư\right)}=0,3\cdot0,1=0,03\left(mol\right)\)
=> \(\hept{\begin{cases}C_{M\left(Al_2\left(SO_4\right)_3\right)}=\frac{0,1}{0,33}\approx0,3\left(M\right)\\C_{M\left(H_2SO_4\right)}=\frac{0,03}{0,33}\approx0,09\left(M\right)\end{cases}}\)