Trộn 200 ml dung dịch gồm Ba(OH)2 0,003M và NaOH 0,001M với 300 ml dung dịch gồm H2SO4 0,0025 M. Tính sự kết tủa và pH của dung dịch
K
Khách
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Những câu hỏi liên quan

8 tháng 9 2019
Đáp án B
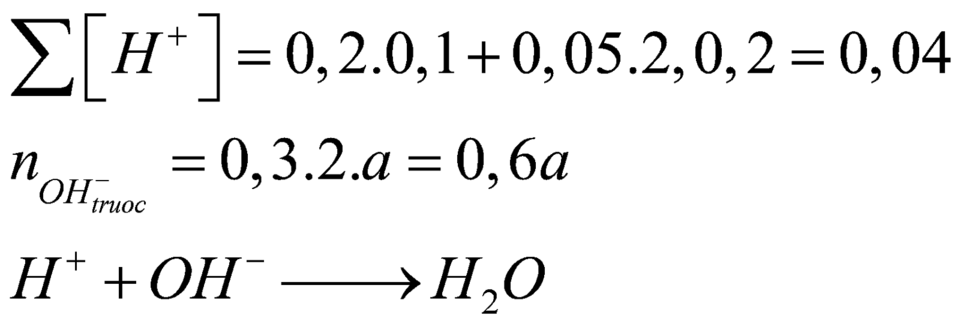
Mà sau phản ứng thu được dung dịch bazo có ph=13 (500ml)nên ta có
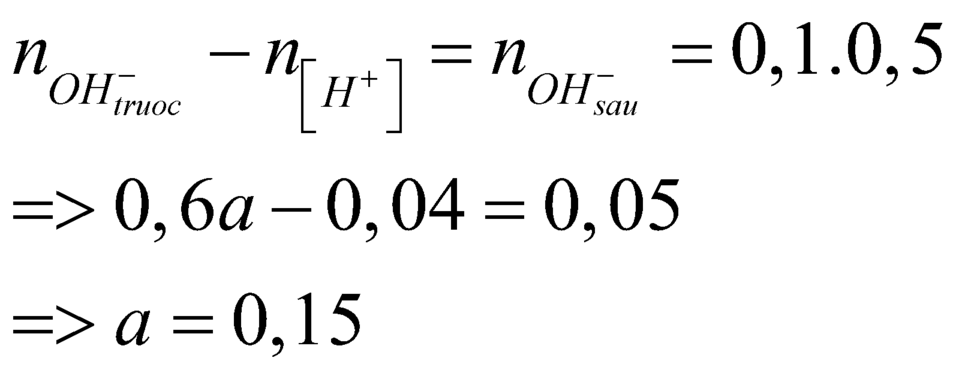
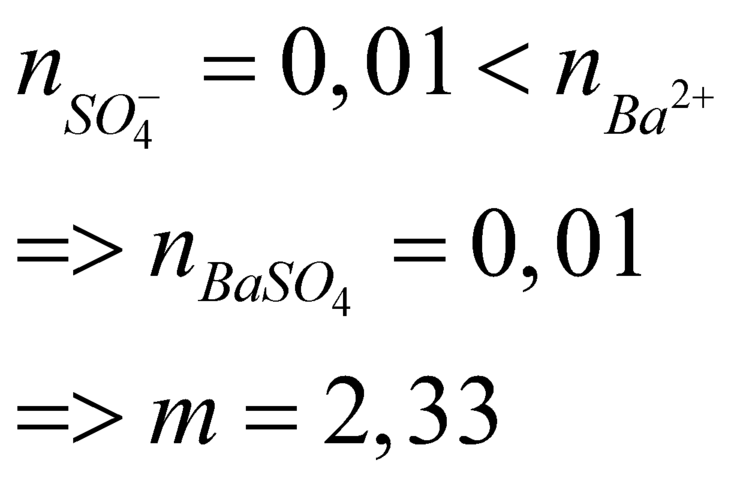

9 tháng 1 2019
Đáp án B
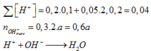
Mà sau phản ứng thu được dung dịch bazo có ph=13 (500ml)nên ta có
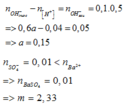



Tính sự kết tủa là tính khối lượng kết tủa thu được hả bạn?
Ta có: \(n_{Ba^{2+}}=n_{Ba\left(OH\right)_2}=0,0006\left(mol\right)\)
\(n_{SO_4^{-2}}=n_{H_2SO_4}=0,0075\left(mol\right)\)
PT ion: \(Ba^{2+}+SO_4^{2-}\rightarrow BaSO_4\downarrow\)
_____ 0,0006__0,0075 → 0,0006 (mol)
\(\Rightarrow m_{BaSO_4}=0,0006.233=0,1398\left(g\right)\)
Ta có: \(n_{OH^-}=2n_{Ba\left(OH\right)_2}+n_{NaOH}=1,4.10^{-3}\left(mol\right)\)
\(n_{H^+}=2n_{H_2SO_4}=1,5.10^{-3}\left(mol\right)\)
PT ion: \(OH^-+H^+\rightarrow H_2O\)
____1,4.10-3 →1,4.10-3______ (mol)
⇒ H+ dư. \(n_{H^+\left(dư\right)}=10^{-4}\left(mol\right)\)
\(\Rightarrow\left[H^+\right]=\frac{10^{-4}}{0,5}=2.10^{-4}M\) \(\Rightarrow pH=-log\left[H^+\right]\approx3,7\)
Bạn tham khảo nhé!