câu 1: áp dụng tính thể tích oxi có trong bình kín có thể tích 0,6l chứa đầy không khí
câu 2: Xác định CTHH của oxit trong các hợp chất sau:
CaO,CaCO3,CO2,SO2,SO3,H2SO4,HNO3,P2O5
Hóa học 8
giúp mik vs
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

câu 1
HBr
đặt b là hóa trị của Br
1.I=1.b
b=I
=>hóa trị của Br=I
tương tự như các ý còn lại

Câu I:
H(I) và Br(I), H(I) và S(II), N(III) và H(I), Si(IV) và H(I), H(I) và SO4 (II), H(I) và PO4(III), H(I) và NO3(I), Na(I) và O(II), Ba(II) và O(II), Al(III) và O(II), C(IV) và O(II), S(VI) và O(II), P(V) và O(II)

Câu 2:
\(CTHH:X_2O_5\\ M_{X_2O_5}=\dfrac{16}{100\%-43,67\%}=142\left(g\text{/}mol\right)\\ \Rightarrow M_X=\dfrac{142-16.5}{2}=31\left(g\text{/}mol\right)\left(P\right)\\ \Rightarrow CTHH:P_2O_5\)
Câu 3:
Trong 1 mol B: \(\left\{{}\begin{matrix}n_{Al}=\dfrac{342.15,79\%}{27}=2\left(mol\right)\\n_S=\dfrac{342.28,07\%}{32}=3\left(mol\right)\\n_O=\dfrac{342-2.27-3.32}{16}=12\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow CTHH_B:Al_2\left(SO_4\right)_3\)
Câu 4:
\(M_X=8,5.2=17\left(g\text{/}mol\right)\)
Trong 1 mol X: \(\left\{{}\begin{matrix}n_N=\dfrac{17.82,35\%}{14}=1\left(mol\right)\\n_H=\dfrac{17.17,65\%}{1}=3\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow CTHH_X:NH_3\)
C1:
\(NaNO3:\)
\(MNaNO3=23+62=\dfrac{85g}{mol}\)
\(\%Na=\dfrac{23.100}{85}=27\%\)
\(\%N=\dfrac{14.100}{85}=16\%\)
\(\%O=\dfrac{16.3.100}{85}=56\%\)
\(K2CO3\)
\(MK2CO3=39.2+60=\dfrac{138g}{mol}\)
\(\%K=\dfrac{39.2.100}{138}=57\%\)
\(\%C=\dfrac{12.100}{138}=9\%\)
\(\%O=\dfrac{16.3.100}{138}=35\%\)
\(Al\left(OH\right)3:\)
\(MAl\left(OH\right)3=27+17.3=\dfrac{78g}{mol}\)
\(\%Al=\dfrac{27.100}{78}=35\%\)
\(\%O=\dfrac{16.3.100}{78}=62\%\)
\(\%H=\dfrac{1.3.100}{78}=4\%\)
\(SO2:\)
\(MSO2=32+16.2=\dfrac{64g}{mol}\)
\(\%S=\dfrac{32.100}{64}=50\%\)
\(\%O=\dfrac{16.2.100}{64}=50\%\)
\(SO3:\)
\(MSO3=32+16.3=\dfrac{80g}{mol}\)
\(\%S=\dfrac{32.100}{80}=40\%\)
\(\%O=\dfrac{16.3.100}{80}=60\%\)
\(Fe2O3:\)
\(MFe2O3=56.2+16.3=\dfrac{160g}{mol}\)
\(\%Fe=\dfrac{56.2.100}{160}=70\%\)
\(\%O=\dfrac{16.3.100}{160}=30\%\)
C5:
a,MX=2,207.29=64đvC
b, gọi cthh của hợp chất này là SxOy
Ta có: 32x:16y=50:50
=>x:y=\(\dfrac{50}{32}:\dfrac{50}{16}\)
= 1,5625:3,125
= 1 : 2
Vậy CTHH của hợp chất này là SO2
C2,3,4 lm r nên t bổ sung thim:>

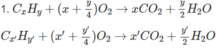
H 2 S O 4 + n H 2 O → H 2 S O 4 .n H 2 O
2NaOH + C O 2 → N a 2 C O 3 + H 2 O
Số mol
C
O
2
là: 
Khối lượng C trong hỗn hợp A là: 0,095.12 = 1,14 (g).
Khối lượng H trong hỗn hợp A là: 1,3 - 1,14 = 0,16 (g).
Số mol
H
2
O
sau phản ứng là: 
Để tạo ra 0,095 mol C O 2 cần 0,095 mol O 2 ;
Để tạo ra 0,08 mol H 2 O cần 0,04 (mol) O 2 .
Số mol O 2 đã tham gia phản ứng là: 0,095 + 0,04 = 0,135 (mol).
Số mol
O
2
ban đầu là: 
Số mol O 2 còn dư là: 0,155 - 0,135 = 0,02 (mol).
Số mol 3 chất trong bình sau phản ứng:
0,095 + 0,08 + 0,02 = 0,195 (mol).
Nếu ở đktc thì V O = 0,195.22,4 = 4,37 (lít).
Thực tế V2 = 8,4 lít
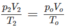
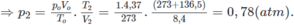
2. Đổi thể tích hỗn hợp khí trước phản ứng về đktc:
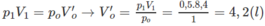
Số mol khí trước phản ứng: 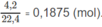
Số mol 2 hiđrocacbon: 0,1875 - 0,155 = 0,0325 (mol).
Đặt lượng C n H 2 n là a mol, lượng C m H 2 m - 2 là b mol, ta có a + b = 0,0325.
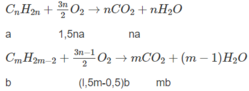
Số mol O 2 : l,5na + (l,5m - 0,5)b = 0,135 (2)
Số mol C O 2 : na + mb = 0,095 (3)
Từ (2) và (3), tìm được b = 0,015 ⇒ a = 0,0175
Thay các giá trị của a và b vào (3), ta có :
1,75. 10 - 2 n + 1,5. 10 - 2 m = 9,5. 10 - 2
7n + 6m = 38
Nếu n = 2 thì 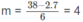
Nếu n = 3 thì 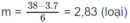
Nếu n > 3 thì m < 2 (loại).
% về thể tích của
C
2
H
4
: 
% về thể tích của C 4 H 6 là 46,2%