Tổng các hạt cơ bản trong một nguyên tử là 155 hạt. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 33 hạt. Số khối của nguyên tử đó là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Số hạt mang điện ( p và e ) là:
( 155 + 33 ) : 2 = 94 ( hạt )
Số hạt ko mang điện ( n ) là:
155 - 94 = 61 ( hạt )
Vì p=e
Hạt P có số hạt là:
94 : 2 = 47 ( hạt )
Xem trong bảng 42 ta được nguyên tố Ag

\(Tổng: 2p+n=155 (1)\\ MĐ > KMĐ: 2p-n=33(2)\\ (1)(2)\\ p=e=47\\ n=61\\ A=47+61=108 (Ag)\)

Giả sử số hiệu nguyên tử, số nơtron trong nguyên tử của nguyên tố X lần lượt là Z, N.
Ta có hpt:
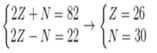
→ Nguyên tử X có số khối: A = Z + N = 26 + 30 = 56
→ Chọn B.

Đáp án B
Giả sử số hiệu nguyên tử, số nơtron trong nguyên tử của nguyên tố X lần lượt là Z, N.
Ta có hệ phương trình :
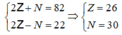
→ Nguyên tử X có số khối:
A = Z + N = 26 + 30 = 56

(Anh làm tóm tắt nha)
Theo đề, ta có HPT:
\(\left\{{}\begin{matrix}2p+n=155\\2p-n=33\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}2n=122\\2p-n=33\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}n=61\\p=47\end{matrix}\right.\)
Vậy p = e = 47 hạt, n = 61 hạt
Ta có số khối của nguyên tử là:
n + p = 61 + 47 = 108 (đvC)

Gọi số proton, notron và số electron của nguyên tử đó là Z, N và Z.

Đáp án A

Đáp án A
Gọi số proton, notron và số electron của nguyên tử đó là Z, N và Z.
⇒ 2 Z + N = 155 2 Z - N = 33 ⇔ Z = 47 N = 61 ⇒ A = Z + N = 108
108