Đốt cháy hoàn toàn 3,2 gam hỗn hợp gồm bột Fe và Mg ( trong đó tỉ lệ số mol nFe : nMg = 1: 3) trong bình chứa oxi thu được m gam chất rắn. Tính phần trăm khối lượng mỗi oxit trong hỗn hợp thu được sau phản ứng.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a)
Gọi n Fe = 3a(mol) ; n Mg = 2a(mol)
Suy ra :
3a.56 + 2a.24 = 21,6
=> a = 0,1
Vậy : n Fe = 0,3 ; n Mg = 0,2(mol)
$3Fe + 2O_2 \xrightarrow{t^o} Fe_3O_4$
$2Mg + O_2 \xrightarrow{t^o} 2MgO$
n Fe3O4 = 1/3 n Fe = 0,1(mol) => m Fe3O4 = 0,1.232 = 23,2(gam)
n MgO = n Mg = 0,2(mol) => m MgO = 0,2.40 = 8(gam)
b)
n O2 = 2/3 n Fe + 1/2 n Mg = 0,3(mol)
V O2 = 0,3.22,4 = 6,72 lít

a)
Theo ĐLBTKL: \(m_{Fe\left(bđ\right)}+m_{O_2}=m_X\)
=> \(m_{O_2}=26,4-20=6,4\left(g\right)\)
=> \(n_{O_2}=\dfrac{6,4}{32}=0,2\left(mol\right)\Rightarrow V=0,2.22,4=4,48\left(l\right)\)
b)
PTHH: 3Fe + 2O2 --to--> Fe3O4
0,2------->0,1
=> \(\%m_{Fe_3O_4}=\dfrac{0,1.232}{26,4}.100\%=87,88\%\)
c)
- Nếu dùng KClO3
PTHH: 2KClO3 --to--> 2KCl + 3O2
\(\dfrac{0,4}{3}\)<-----------------0,2
=> \(m_{KClO_3}=\dfrac{0,4}{3}.122,5=\dfrac{49}{3}\left(g\right)\)
- Nếu dùng KMnO4:
PTHH: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
0,4<--------------------------------0,2
=> \(m_{KMnO_4}=0,4.158=63,2\left(g\right)\)

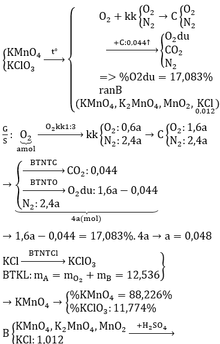
Gọi số mol C, S là a, b
=> 12a + 32b = 7,68
PTHH: C + O2 --to--> CO2
_____a--------------->a
S + O2 --to--> SO2
b--------------->b
=> a + b = \(\dfrac{9,856}{22,4}=0,44\)
=> a = 0,32; b = 0,12
=> \(\left\{{}\begin{matrix}\%C=\dfrac{0,32.12}{7,68}.100\%=50\%\\\%S=\dfrac{0,12.32}{7,68}.100\%=50\%\end{matrix}\right.\)

Đáp án A
Trong các sản phẩm khử có H2 nên NO3- hết
Sau khi tác dụng với NaOH thì dung dịch thu được chỉ gồm NaCl là KCl
→ nHCl = nNaCl + nKCl = nNaOH + nKNO3 = 0,9mol
Bảo toàn H có nHCl = 2nH2 + 4nNH4 + 2nH2O
→ nH2O = 0,4 mol
BTKL : mA + mHCl + mKNO3 = mmuối + mH2O + mC
→ mA = 20,6 gam
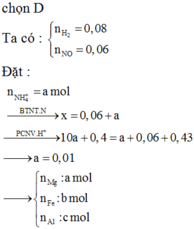
Đặt a, b,c, d lần lượt là số mol của Mg, MgCO3, Fe, Fe(NO3)2
Có mA = 24a + 84b + 56c + 180d =20,6
nO = 3b+ 6d = 20,6. %O : 16 = 0,48
mmuối = 24(a+b) + 56(c + d ) + 0,07.39 + 0,01.18 + 0,09.35,5 = 45,74
moxit = 40 (a +b ) + 160 (c + d ) . ½ = 17,6
Giải hệ được a =0,26; b = 0,1; c= 0,01; d=0,03
→ %Fe = 2,7 %
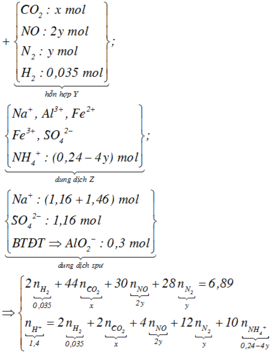
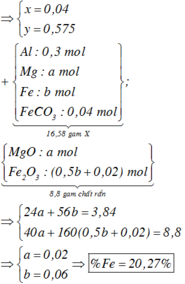
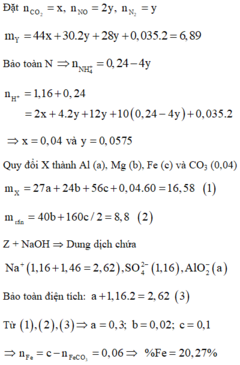
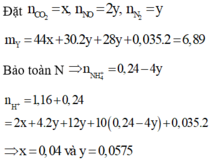


Gọi \(n_{Fe}=x\left(mol\right)\Rightarrow m_{Fe}=56x\left(g\right)\)
\(n_{Mg}=3x\left(mol\right)\Rightarrow m_{Mg}=72x\left(g\right)\)
\(m_{Fe}+m_{Mg}=3,2\)
=>\(56x+72x=3,2\)
\(\Rightarrow128x=3,2\)
\(\Rightarrow x=0,025\)
\(3Fe+2O2-->Fe3O4\)
0,025------------------1/120(mol)
\(2Mg+O2-->2MgO\)
0,075------------------0,075(mol)
\(m_{hh}=\frac{1}{120}.232+0,075.40=\frac{74}{15}\left(g\right)\)
\(\%m_{Fe3O4}=\frac{\frac{29}{15}}{\frac{74}{15}}.100\%=38,67\%\)
\(\%m_{MgO}=100-38,67=61,33\%\)
T chắc chắn Duong Le chuyên H2