1.Cho 3,2 gam một kim loại M tác dụng vừa đủ với khí clo thu được 6,75 gam muối. Tìm M
2.Cho 2,24 lit halogen X2 ở đktc tác dụng vừa đủ với Cu thu được 22,4 gam muối. X là:
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_M=\dfrac{7,2}{M_M}\left(mol\right)\)
PTHH: M + Cl2 --to--> MCl2
\(\dfrac{7,2}{M_M}\)------------>\(\dfrac{7,2}{M_M}\)
=> \(\dfrac{7,2}{M_M}\left(M_M+71\right)=28,5=>M_M=24\left(Mg\right)\)

Đáp án D
Có

m g X + HNO3 đặc nguội → 0,1 mol NO2
→ BTe a . n M = 0 , 1 m o l ( 2 )
Từ (1) và (2) suy ra:
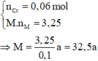
=> a = 2, M = 65 (M là Zn).

PTHH: \(R+Cl_2\xrightarrow[]{t^o}RCl_2\)
Theo PTHH: \(n_R=n_{RCl_2}\)
\(\Rightarrow\dfrac{12,8}{R}=\dfrac{27}{R+71}\) \(\Leftrightarrow R=64\) (Đồng)

Gọi halogen đó là X , CTTQ: CuX2
\(PTHH:Cu+X_2\underrightarrow{^{to}}CuX_2\)
Áp dụng ĐLTL ta có:
\(\Leftrightarrow\frac{22,4}{5,6}=\frac{64+2X}{33,75}\)
\(\Rightarrow x=35,5\left(Clo\right)\)
Vậy halogen là Clo ( Clo )
1.
Gọi hóa trị của kim loại M là n, ta có:
\(2M+nCl_2\underrightarrow{^{to}}2MCl_n\)
Dựa vào pt, ta thấy:
nM=nMCln
⇔ 3,2/M=6,75/M+35,5n
⇔ M=32n
Vì M là kim loại nên hóa trị có thể là I, II và III:
- Nếu n=1 ==> M=32 (Loại)
- Nếu n=2 ==> M=64 (Chọn - Cu)
- Nếu n=3 ==> M=96 (Loại)
Vậy kim loại M là Cu.
2.
\(Cu+X_2\underrightarrow{^{to}}CuX_2\)
nX2=2,24/22,4=0,1 (mol)
nCuX2=nX2=0,1 (mol)
==> mCuX2= 0,1.(64 + 2X)=22,4
==> X= 80 (Br)
Vậy halogen X là Br.