Bài : Hòa tan hoàn toàn a gam kim loại M trong dung dịch HCl thu được dung dịch A và 2.24 lít H2 (đktc). CHia A thành 2 phần bằng nhau : Phần thứ nhất tác dụng hoàn toàn với KOH dư , thu được kết tủa B . Nung B trong không khí ở nhiệt độ cao tới khối lượng không đổi , thu được (b+2.4) gam chất rắn C . Hòa tan C trong H2SO4 loãng dư được dung dịch D . Xử lí D ở nhiệt độ thích hợp thu được 28.1 gam 1 muối duy nhất . Xử lí phần 2 chỉ thu được một muối Y duy nhất với khối lượng 19.9 gam . Xác định công thức X , Y biết a=2b
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
P1: nFe(OH)2 = 3,6/90 = 0,04 mol => nFe2+ = 0,04 mol
P2:
Fe2+: x mol
H+: y mol
Cl-: 2x + y
3Fe2+ + 4H+ + NO3- → 3Fe3+ + NO + 2H2O
0,06 ← 0,08 ← 0,02
=> y = 0,08
Fe2+ + Ag+ → Fe3+ + Ag
x-0,06 → x-0,06
Ag+ + Cl- → AgCl
2x+y → 2x+y
=> 108(x-0,06) + 143,5(2x+y) = 68,2 => x = 0,16
=> nFe phản ứng ban đầu = nH2 = 0,04+0,16 = 0,2 mol => VH2 = 4,48 lít

Đáp án A
P1: nFe(OH)2 = 3,6/90 = 0,04 mol
=> nFe2+ = 0,04 mol
P2:
Fe2+: x mol
H+: y mol
Cl-: 2x + y
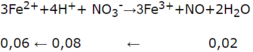
=> y = 0,08
Fe2++Ag+→Fe3++Ag
x-0,06 → x-0,06
Ag+ + Cl- → AgCl
2x+y → 2x+y
=> 108(x-0,06) + 143,5(2x+y) = 68,2 => x = 0,16
=> nFe phản ứng ban đầu = nH2 = 0,04+0,16 = 0,2 mol => VH2 = 4,48 lít

P1: nFe(OH)2 = 3,6/90 = 0,04 mol => nFe2+ = 0,04 mol
P2:
Fe2+: x mol
H+: y mol
Cl-: 2x + y
3Fe2+ + 4H+ + NO3- → 3Fe3+ + NO + 2H2O
0,06 ← 0,08 ← 0,02
=> y = 0,08
Fe2+ + Ag+ → Fe3+ + Ag
x-0,06 → x-0,06
Ag+ + Cl- → AgCl
2x+y → 2x+y
=> 108(x-0,06) + 143,5(2x+y) = 68,2 => x = 0,16
=> nFe phản ứng ban đầu = nH2 = 0,04+0,16 = 0,2 mol => VH2 = 4,48 lít
Đáp án A

Chọn A
Vì: P1: nFe(OH)2 = 3,6/90 = 0,04 mol => nFe2+ = 0,04 mol
P2: Fe2+: x mol
H+: y mol
Cl-: 2x + y
3Fe2+ + 4H+ + NO3- → 3Fe3+ + NO + 2H2O
0,06 ← 0,08 ← 0,02
=> y = 0,08
Fe2+ + Ag+ → Fe3+ + Ag
x-0,06 → x-0,06
Ag+ + Cl- → AgCl
2x+y → 2x+y
=> 108(x-0,06) + 143,5(2x+y) = 68,2 => x = 0,16
=> nFe phản ứng ban đầu = nH2 = 0,04+0,16 = 0,2 mol
=> VH2 = 4,48 lít



Qui đổi ½ hh B gồm Al (x mol), Fe (y mol), O (z mol)

=> mB = 2 (mAl + mFe + mO) = 102,78g
Gọi công thức của oxit sắt là FeaOb

=> Fe2O3

\(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
- Nếu B là muối khan
PTHH: 2R + 2nHCl --> 2RCln + nH2
\(\dfrac{0,2}{n}\) <----- \(\dfrac{0,2}{n}\)<--0,1
- Nếu B là muối khan
=> \(M_{RCl_n}=\dfrac{19,9}{\dfrac{0,2}{n}}=99,5n\left(g/mol\right)\)
=> MR = 64n (g/mol)
Với mọi n --> Không có TH thỏa mãn => Loại
=> B là muối ngậm nước
\(n_{RCl_n.xH_2O}=\dfrac{0,2}{n}\left(mol\right)\)
=> \(M_R+35,5n+18x=99,5n\)
=> MR = 64n - 18x (1)
Chất rắn D là oxit của R
Giả sử D có CTHH: R2Oy
Bảo toàn R: \(n_{R_2O_y}=\dfrac{0,1}{n}\left(mol\right)\)
=> \(m_{R_2O_y}=\dfrac{0,1}{n}\left(2.M_R+16y\right)\)
=> \(\dfrac{0,1}{n}\left(2.M_R+16y\right)=m+2,4=\dfrac{0,2}{n}.M_R+2,4\)
=> \(\dfrac{1,6y}{n}=2,4\)
=> \(\dfrac{y}{n}=\dfrac{3}{2}\) => Chọn y = 3; n = 2
(1) => MR = 128 - 18x (g/mol)
Chỉ có x = 4 thỏa mãn => MR = 56 (g/mol)
=> R là Fe
B là FeCl2.4H2O
\(n_{Fe_2O_3}=\dfrac{m+2,4}{160}=\dfrac{5,6+2,4}{160}=0,05\left(mol\right)\)
PTHH: Fe2O3 + 3H2SO4 --> Fe2(SO4)3 + 3H2O
0,05----------------->0,05
G có dạng Fe2(SO4)3.qH2O
=> \(n_{Fe_2\left(SO_4\right)_3.qH_2O}=0,05\left(mol\right)\)
=> \(M_{Fe_2\left(SO_4\right)_3.qH_2O}=\dfrac{28,2}{0,05}=564\left(g/mol\right)\)
=> q = 9,11 (L)
=> Không tìm đc G, bn check đề nhé :)
\(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH: 2R + 2xHCl ---> 2RClx + xH2
\(\dfrac{0,2}{x}\) 0,2 \(\dfrac{0,2}{x}\) 0,1
Áp dụng ĐLBTKL:
\(m_R+m_{HCl}=m_{RCl_x}+m_{H_2}\\ \rightarrow m_R=19,9+0,1.2-0,2.36,5=12,8\left(g\right)\)
\(\rightarrow M_R=\dfrac{12,8}{\dfrac{0,2}{x}}=64x\left(\dfrac{g}{mol}\right)\)
Xét x = 1 thoả mãn => R là Cu
Bạn ơi sai đề à Cu ko pư vs HCl :)?






Đây mà là toán 1 hở
phải mà là phần 1