Cho 6,72 lít hỗn hợp gồm metan, etilen và axetilen (đkc) được dẫn qua dung dịch AgNO3/NH3 dư thấy có 12 gam kết tủa vàng nhạt. Hỗn hợp khí còn lại dẫn tiếp tục qua nước brom, thấy khối lượng bình này tăng thêm 4,2 gam. Xác định %V các khí trong hỗn hợp ban đầu.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(V_{C_2H_6}=13,44-6,72=6,72\left(l\right)\)
=> \(n_{C_2H_6}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(n_{C_2Ag_2}=\dfrac{24}{240}=0,1\left(mol\right)\)
=> \(n_{C_2H_2}=0,1\left(mol\right)\)
=> \(n_{C_2H_4}=\dfrac{13,44}{22,4}-0,3-0,1=0,2\left(mol\right)\)
=> \(\left\{{}\begin{matrix}\%m_{C_2H_6}=\dfrac{0,3.30}{0,3.30+0,2.28+0,1.26}.100\%=52,326\%\\\%m_{C_2H_4}=\dfrac{0,2.28}{0,3.30+0,2.28+0,1.26}.100\%=32,558\%\\\%m_{C_2H_2}=\dfrac{0,1.26}{0,3.30+0,2.28+0,1.26}.100\%=15,116\%\end{matrix}\right.\)

CH2=CH2 + Br2 → CH2Br-CH2Br
CH≡CH + Br2 → CHBr2-CHBr2
CH≡CH + 2AgNO3 + 2NH3 → AgC≡CAg↓vàng + 2NH4NO3
Khí không bị hấp thụ (hay không có phản ứng) là khí propan (C3H8)

nhh = 5.6/22.4 = 0.25(mol)
nAg2C2 = nC2H2 = 24/240 = 0.1 (mol)
nBr2 = 0.3 (mol)
=> nC2H4 = 0.3 - 0.1*2 = 0.1 (mol)
nCH4 = 0.25 - 0.1 - 0.1 = 0.05 (mol)
mCH4 = 0.05*16 = 0.8 (g)
mC2H2 = 0.1*26 = 2.6 (g)
mC2H4 = 0.1*28 = 2.8 (g)
mhh = 0.8 + 2.6 + 2.8 = 6.2 (g)
%CH4 = 0.8/6.2 * 100% = 12.9%
%C2H4 = 2.8/ 6.2 * 100% = 45.16%
%C2H2 = 41.94%

Đáp án C
C2H2 và C2H4 cho qua dd AgNO3 chỉ có C2H2 phản ứng => khí đi ra là khí C2H4
BTNT C: nC2H2 = nAg2C2 = 28,8: 240 = 0,12 (mol)
nC2H4 = 2,912 : 22,4 = 0,13 (mol)
%m C2H2 = (mC2H2 : mhh khí).100% = [ 0,12. 26 : (0,12.26 + 0,13.28)].100% = 46,15%

ĐÁP ÁN B
Chỉ có C2H2 phản ứng tạo Ag2C2 => nkhí = nC2H4 = 0,13 mol
,nAg2C2 = nC2H2 = 0,12 mol
=> %mC2H2 = 46,15%

Ta có: \(n_X=\dfrac{3,584}{22,4}=0,16\left(mol\right)\)
- Cho hh khí quá bình 1:
PT: \(C_3H_4+AgNO_3+NH_3\rightarrow AgC_3H_3+NH_4NO_3\)
Ta có: \(n_{AgC_3H_3}=\dfrac{5,88}{147}=0,04\left(mol\right)\)
Theo PT: \(n_{C_3H_4}=n_{AgC_3H_3}=0,04\left(mol\right)\)
- Cho tiếp hh khí còn lại qua bình 2, thấy dd Br2 nhạt màu.
→ Br2 dư, C2H4 pư hết. Khí thoát ra là C3H8.
PT: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
Ta có: \(n_{C_3H_8}=\dfrac{1,792}{22,4}=0,08\left(mol\right)\)
a, \(\left\{{}\begin{matrix}\%V_{C_2H_4}=\dfrac{0,16-0,08-0,04}{0,16}.100\%=25\%\\\%V_{C_3H_4}=\dfrac{0,04}{0,16}.100\%=25\%\\\%V_{C_3H_8}=50\%\end{matrix}\right.\)
b, Ta có: \(n_X=\dfrac{1,792}{22,4}=0,08\left(mol\right)\)
\(\Rightarrow X\left\{{}\begin{matrix}n_{C_2H_4}=0,08.25\%=0,02\left(mol\right)\\n_{C_3H_4}=0,08.25\%=0,02\left(mol\right)\\n_{C_3H_8}=0,04\left(mol\right)\end{matrix}\right.\) \(\Rightarrow n_{\pi}=n_{C_2H_4}+2n_{C_3H_4}=0,06\left(mol\right)\)
\(n_{Br_2}=0,08.1=0,08\left(mol\right)\)
⇒ nπ < nBr2
→ Br2 dư. Hiện tượng: Dd Br2 nhạt màu dần.

Khi dẫn X qua AgNO3/NH3 thì chỉ có propin phản ứng
CHΞC-CH3 + AgNO3 + NH3 → AgCΞC-CH3 ↓ + NH4NO3
nAgCΞC-CH3 = \(\dfrac{29,4}{147}\)= 0,2 mol = nPropin
Nếu dẫn X qua bình đựng dd brom dư thì khối lượng bình tăng = mPropin + m Etilen
<=> 12,2 = mPropin + m Etilen
<=> 0,2.40 + mEtilen = 12,2
<=> mEtilen = 4,2 gam => nEtilen = 4.2:28 = 0,15 mol
nX = 10,08 : 22,4 = 0,45 mol
=> %V Etilen = \(\dfrac{0,15}{0,45}\).100% = 33,33%
%V Propin = \(\dfrac{0,2}{0,45}\).100% = 44,44%
=> %V Metan = 100 - 33,33 - 44,44 = 22,23%
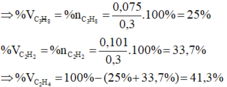
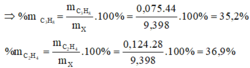

\(n_{hh}=0,3\left(mol\right);n_{C_2Ag_2}=0,05\left(mol\right);n_{C_2H_4}=0,15\left(mol\right)\\ n_{C_2H_2}=n_{C_2Ag_2}=0,05\left(mol\right)\\ \Rightarrow n_{CH_4}=0,3-0,05-0,15=0,1\left(mol\right)\)
\(\Rightarrow\%C_2H_2=16,67\%\\ \%CH_4=33,33\%\\ \%C_2H_4=50\%\)
làm sao tìm đc nC2H4 vậy ạ?