Bài 1:
Đặt cốc A đựng dung dịch HCl và cốc B đựng dung dịch H2SO4 loãng lên 2 đĩa cân sao cho cân ở vị trí cân bằng. Tiếp đến thực hiện các thí nghiệm sau đây:
- Cho 5,6 g Fe vào cốc đựng dung dịch HCl.
- Cho a gam Al vào cốc đựng dung dịch H2SO4.
Khi cả Fe và Al đều tan hoàn toàn thấy cân ở vị trí thăng bằng. Hãy tính a?
Bài 2. Cho 38,168 ml dung dịch H2SO4 19,6% (d =1,31 g/ml) vào 208 gam dung dịch BaCl2 10%.
a. Viết PTPU xảy ra và tính khối lượng kết tủa tạo ra sau PU.
b.Tính nồng độ phần trăm của dung dịch thu được sau phản ứng khi đã loại bỏ hết kết tủa.
Bài 3. Dẫn khí CO dư qua ống đựng bột một oxit sắt (FexOy) ở nhiệt độ cao. Sau khi phản ứng kết thúcthu được 0,84 gam sắt và dẫn khí sinh ra vào nước vôi trong dư thì thu được 2 gam kết tủa. Xác định công thức phân tử của FexOy.

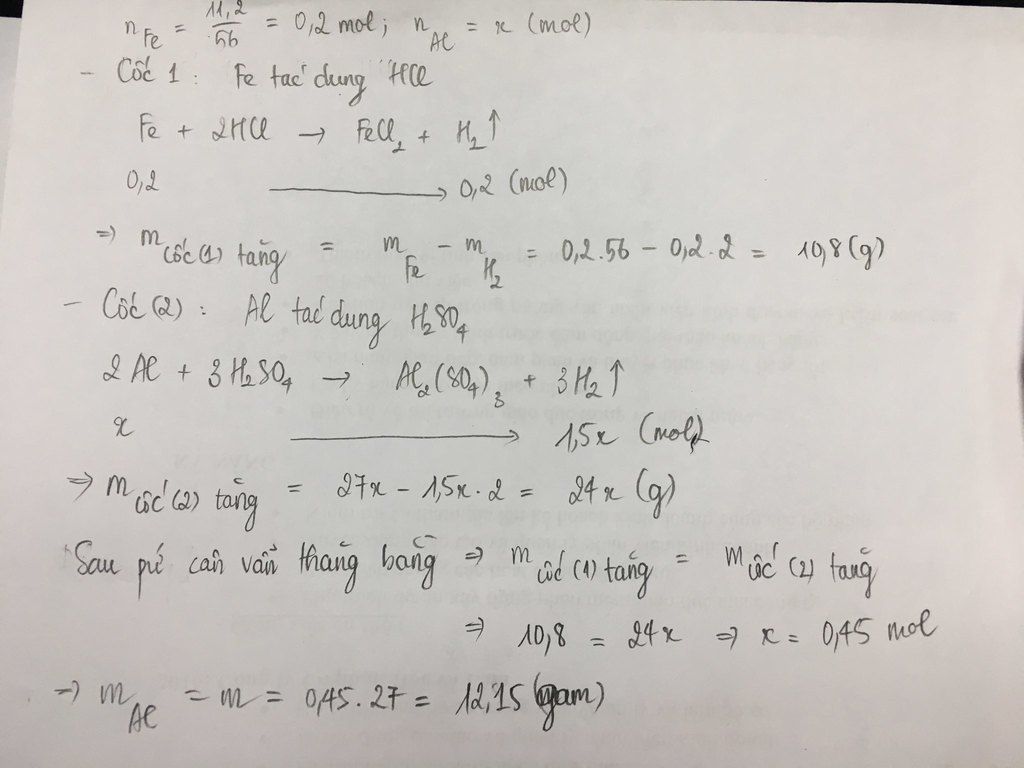


Bài 1
\(n_{Fe}=\frac{5,6}{56}=0,1\left(mol\right)\)
\(n_{Al}=\frac{a}{27}\left(mol\right)\)
TN1: \(Fe+2HCl-->FeCl2+H2\)
----0,1-------0,2------------------0,1---0,1(mol)
dd sau pư là FeCl2 và có thể có HCl dư
TN2 : \(2Al+3H2SO4-->Al2\left(SO4\right)3+3H2\)
-------a/27-----\(\frac{a}{40,5}\)---------------------\(\frac{a}{13,5}\)-----------\(\frac{a}{40,5}\)(mol)
dd sau pư là Al2(SO4)3 và có thể có thêm H2SO4
Vì sau khi phản ứng cái kim đồng hồ cân nặng vẫn ở vị trí cân bằng nên ta có
\(m_{Fe}-m_{H2}=m_{Al}-m_{H2}\)
\(\Leftrightarrow5,6-0,2=a-\frac{a}{20,25}\)
\(\Leftrightarrow5,4=\frac{19,25a}{20,25}\)
\(\Leftrightarrow109,35=19,25a\)
\(\Rightarrow a\approx5,68\)(g)
Bài 2
\(H2SO4+BaCl2-->BaSO4+2HCl\)
a) Ta có
\(n_{H2SO4}=\frac{38,168.19,6\%}{98}=0,08\left(g\right)\)
\(n_{BaCl2}=\frac{208.10\%}{208}=0,1\left(mol\right)\)
=> BaCl2 dư. Muối sau pư là BaCl2 dư
\(n_{BaSO4\downarrow}=n_{H2SO4}=0,08\left(mol\right)\)
\(m_{BaSO4}=0,08.233=18,64\left(g\right)\)
\(n_{BaCl2}=n_{H2SO4}=0,08\left(mol\right)\)
\(\Rightarrow n_{BaCl2}dư=0,1-0,08=0,02\left(mol\right)\)
\(m_{BaCl2}=0,02.208=4,16\left(g\right)\)
b) dd sau pư là BaCl2 dư và HCl
\(mdd=m_{ddH2SO4}+m_{ddBaCl2}-m_{BaSO4}=38,168+208-18,64=227,528\left(g\right)\)
\(m_{HCl}=0,08.36,5=2,92\left(g\right)\)
\(C\%_{HCl}=\frac{2,92}{277,528}.100\%=1,05\%\)
\(C\%_{BaCl2}dư=\frac{4,16}{277,528}.100\%=1,5\%\)
bài 3