đốt cháy 9,92 gam photpho trong bình chứa 13,44 lít khí oxi ( đktn).
a) viết phương trình hóa học xảy ra
b) sau khi cháy chất nào còn dư? dư bao nhiêu?
c)chất nào được tạo thành? khối lượng là bao nhiêu?
Mọi người giúp mình với ạ mình xin cảm ơn nhiều...


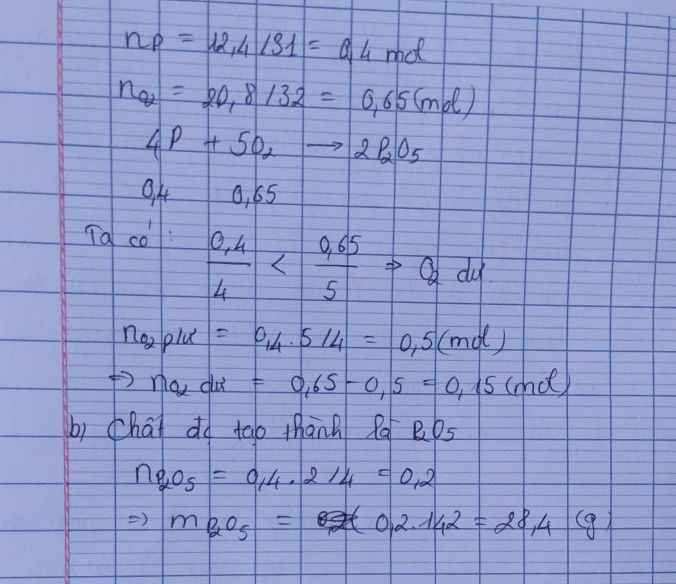
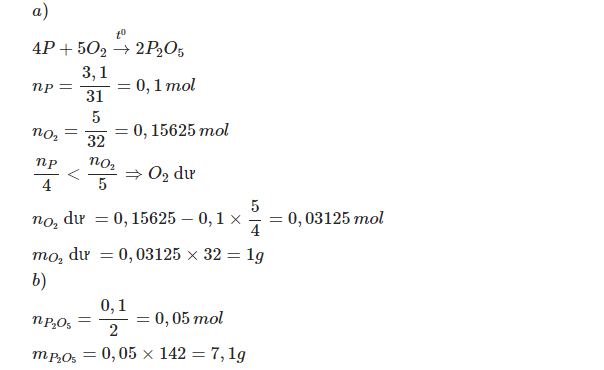
\(4P+5O2-->2P2O5\)
b) \(n_P=\frac{9,92}{31}=0,32\left(mol\right)\)
\(n_{O2}=\frac{13,44}{22,4}=0,6\left(mol\right)\)
\(\Rightarrow02dư\)
\(n_{O2}=\frac{5}{4}n_P=0,4\left(mol\right)\)
\(n_{O2}dư=0,6-0,4=0,2\left(mOL\right)\)
\(mO2dư=0,2.32=6,4\left(g\right)\)
c) Chất tạo thành là P2O5
n\(P2O5=\frac{1}{2}n_P=0,16\left(mol\right)\)
\(mP2O5=0,16.142=22,72\left(g\right)\)