Hoà tan hoàn toàn 19 gam MgCl2 với một dung dịch NaOH đủ sau phản ứng thu được kết tủa và một muối tan. Lọc lấy kết tủa sau đó nung kết tủa đến khi khối lượng không đổi thu được m gam chất rắn .
a) Viết các phương trình hoá học xảy ra
b) Tính m .
c) Tính khối lượng chất tan có trong nước lọc .
(cho biết nguyên tử khối của: Mg = 24 , Cl = 35,5 , Na = 23 , O = 16 , H = 1 )




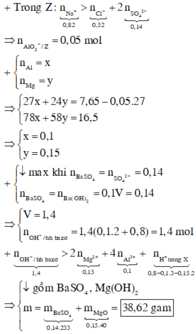



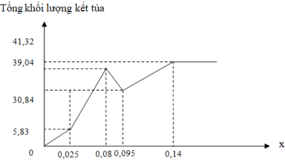
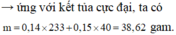
a) MgCl2+2NaOH--->Mg(OH)2+2NaCl
Mg(OH)2--->MgO+H2O
b) n MgCl2=19/95=0,2(mol)
Theo pthh1
n Mg(OH)2=n MgCl2=0,2(mol)
Theo pthh2
n MgO=n Mg(OH)2=0,2(MOL)
m=m MgO=0,2.40=8(g)
c) n NaCl=2n MgCl2=0,4(mol)
m NaCl=0,4.58,5=23,4(g)