Bài 14: Những chất nào trong mỗi dãy sau có hàm lượng (thành phần phần trăm theo khối lượng) oxi cao nhất, thấp nhất
a) FeO; Fe2O3; Fe3O4
a) NO; NO2; N2O; N2O5
a) KMnO4; KClO3; KNO3
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) FeO;Fe2O3;Fe3O4
=> %O=\(\frac{16}{72}.100=22,2\%\)
=>%O=\(\frac{16.3}{160}.100=30\%\)
=>%O=\(\frac{16.4}{232}.100=27,5\%\)
=>thành phần %oxi cao nhất là Fe2O3, thấp nhất là FeO
b)NO;NO2;N2O;N2O5
=> %O=\(\frac{16}{30}.100=53,3\%\)
=>%O=\(\frac{16.2}{46}.100=69,9\%\)
=>%O=\(\frac{16}{44}.100=36,4\%\)
=>%O=\(\frac{16.5}{108}.100=74,1\%\)
thành phần %oxi cao nhất là N2O5, thấp nhất là N2O

a. Trong KMnO4
%mO4=(16x4):(39+55+16x4)x100%=40,51%
Tương tụ ta có : trong KClO3: 39,18%
trong KNO3: 47,52%
Ta có:
\(\%m_O\left(KMnO_4\right)=\frac{16\times4}{39+55+16\times4}\times100\%=40,506\%\)
\(\%m_O\left(KClO_3\right)=\frac{16\times3}{39+35,5+16\times3}\times100\%=39,184\%\)
\(\%m_O\left(KNO_3\right)=\frac{16\times3}{39+14+16\times3}\times100\%=47,525\%\)
Vậy:
+) Chất có hàm lượng oxi cao nhất là KNO3
+) Chất có hàm lượng oxi thấp nhất là KClO3

Đáp án A.
Hợp chất khí với Hidro của R có công thức là RHx ( 4
≥
x
≥
1) => Oxit cao nhất của R là ![]() . Theo đề bài ta có:
. Theo đề bài ta có:

Ta có:
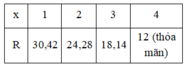
Vậy R là C
=> Hợp chất khí với Hidro là CH4 và Oxit cao nhất là CO2
Nhận xét các đáp án:
A đúng: Do CO2 có cấu trúc mạch thẳng O – C – O nên lực hút của nguyên tử Oxi triệt tiêu lẫn nhau CO2 có liên kết cộng hóa trị giữa nguyên tử C và O phân cực nhưng phân tử CO2 không phân cực.
B sai: Ở điều kiện thường CO2 là hợp chất khí.
C sai: Trong bảng tuần hoàn C thuộc chu kì 2.
D sai: Ở trạng thái cơ bản C có 4 electron s.
Bạn tham khảo tại đây :
Ý a , b :Câu hỏi của LIÊN - Hóa học lớp 8 | Học trực tuyến
Ý c :Câu hỏi của Phù Thủy - Hóa học lớp 8 | Học trực tuyến
a)
- FeO có PTK=56+16=72
⇒%O=\(\frac{16}{72}\). 100=22,2%
-Fe2O3 có PTK=56.2+16.3=160
⇒%O =\(\frac{16.3}{160}\).100= 30%
-Fe3O4 có PTK= 56.3+16.4=232
⇒O%=\(\frac{16.4}{232}\).100= 27,5%
=>Thành phần %O cao nhất là Fe2O3, thấp nhất là FeO
b)
-NO có PTK=14+16=30
⇒%O=\(\frac{16}{30}\).100= 53,3%
-NO2 có PTK=14+ 16.2=46
⇒%O=\(\frac{16.2}{46}\).100= 69,5%
-N2O có PTK= 14.2+16=44
⇒%O=\(\frac{16}{44}\).100=36,36%
-N2O5 có PTK=14.2+16.5=108
⇒%O=\(\frac{16.5}{108}\).100=74,074%
=>Thành phần %O cao nhất là N2O5, thấp nhất là N2O
c)
-KMnO4 có PTK=39+55+16.4=158
⇒%O=\(\frac{16.4}{158}\)100=40,5%
-KClO2 có PTK= 39+35,5+ 16.2=106,5
⇒%O=\(\frac{16.2}{106,5}\).100=30,04%
-KNO3 có PTK= 39+14+16.3=101
⇒%O=\(\frac{16.3}{101}\).100=47,5%
⇒Thành phần %O cao nhất là KNO3, thấp nhất là KClO2