hòa tan hoàn toàn 14,8g hỗn hợp kim loại X có hóa trị 1 và kim loại Y có hóa trị 2 vào nước, sau phản ứng thu được 4,48 lít khí H2 đktc và 5,6g chất rắn không tan. Xác định kim loại X và Y biết số mol X gấp 4 lần số mol Y
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án : D
Dung dịch X chỉ chứa 1 chất tan duy nhất
=> kim loại hóa trị 2 tan trong kiềm
Gọi kim loại kiềm là X và kim loại hóa trị 2 là Y
=> X + H2O -> XOH + ½ H2
2XOH + YO -> X2YO2 + H2O
=> 2nH2 = nX = nXOH = 0,4 mol
=> nX2YO2 = ½ nX = 0,2 mol
=> CM = 0,4M

Đáp án A
M → Mn+ + ne
1,25 → 1,25nx
Zn → Zn2+ + 2e
x → 2x
Cl2 + 2e → 2Cl-
0,2 → 0,4
2H+ + 2e → H2
0,5 ← 0,25
BT e ⇒1,25nx + 2x = 0,4 + 0,5 = 0,9 (1)
Mặt khác: 1,25M + 65M = 19 (2)
(1)(2) ⇒ (1,25M +65)/(1,25n + 2) = 19/0,9 ⇒ n = 2; M = 24(Mg)

Đáp án A
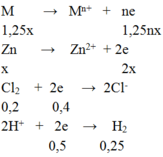
Bảo toàn e ⇒1,25nx + 2x = 0,4 + 0,5 = 0,9 (1)
Mặt khác: 1,25M + 65M = 19 (2)
Từ (1) và (2) ⇒ (1,25M +65M)/(1,25n + 2) = 19/0,9 ⇒ n = 2; M = 24(Mg)

Chuyển đổi hết từ khối lượng chất sang mol chất, rồi viết phương trình phản ứng , tính từng bước theo phương trình hóa học sẽ ra được.

Khi hòa tan hoàn toàn hỗn hợp X và Y vào nước thu được 4,48l H2 và 5,6 g chất rắn không tan.
Chứng tở trong X và Y có một kim loại không tan trong nước
14,8 gam hỗn hợp gồm: \(\left\{{}\begin{matrix}X:4a\left(mol\right)\\Y:a\left(mol\right)\end{matrix}\right.\)
\(TH1:\)X tan được trong nước, Y không tan trong nước:
Khi hòa tan hỗn hợp trên vào nước thì:
\(2X+2H_2O--->2XOH+H_2\)\((1)\)
\(nH_2=\dfrac{4,48}{22,4}=0,2(mol)\)
Theo PTHH (1) \(nH_2=\dfrac{1}{2}.nX=2a(mol)\)
\(=>2a=0,2\)
\(=>a=0,1\)
\(\Rightarrow\left\{{}\begin{matrix}nX=4a=0,4\left(mol\right)\\nY=a=0,1\left(mol\right)\end{matrix}\right.\)
Khối lượng hỗn hợp trên là 14,8 gam, ta có:
\(0,4X+0,1Y=14,8\)\((I)\)
Chất rắn không tan là Y:
\(=>0,1Y=5,6\) \((II)\)
Từ (I) và (II) \(\left\{{}\begin{matrix}0,4X+0,1Y=14,8\\0,1Y=5,6\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}X=23\left(Na\right)\\Y=56\left(Fe\right)\end{matrix}\right.\) (Thõa mãn)
\(TH2:\)Y là kim laoij tan trong nước, X không tan trong nước:
Khi hòa tan hỗn hợp trên vào nước thì:
\(Y+2H_2O--->Y(OH)_2+H_2\)\((2)\)
\(nH_2=\dfrac{4,48}{22,4}=0,2(mol)\)
Theo PTHH (2) \(nH_2=nY=a(mol)\)
\(=>a=0,2\)
\(\Rightarrow\left\{{}\begin{matrix}nX=4a=0,8\left(mol\right)\\nY=a=0,2\left(mol\right)\end{matrix}\right.\)
Khối lượng hỗn hợp trên là 14,8 gam, ta có:
\(0,8X+0,2Y=14,8\)\((III)\)
Chất rắn không tan là X:
\(=>0,8X=5,6\)\((IV)\)
Từ (III) và (IV): \(\left\{{}\begin{matrix}0,8X+0,2Y=14,8\\0,8X=5,6\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}X=7\\Y=46\end{matrix}\right.\) (loại)
Vậy kim loại X là \(Na\), Y là \(Fe\).





tham khảo nha
a là gì vậy bạn sao nH2 lại bằng 2a