Nhiệt phân hoàn toàn 4,385 gam hỗn hợp X gồm KClO3 và KMnO4, thu được O2 và m gam chất rắn Y gồm K2MnO4, MnO2 và KCl. Toàn bộ lượng O2 thu được cho tác dụng hết với cacbon nóng đỏ, thu được 0,896 lít (ở đktc) hỗn hợp khí Z (gồm CO và CO2) có tỉ khối so với H2 bằng 16.ư
a) Tính khối lượng của các chất trong X.
b) Tính thể tích (ở đktc) khí Cl2 thu được khi cho 8,77 gam X (ở trên ) tác dụng hết với dung dịch axit HCl đặc, dư (có đun nóng).

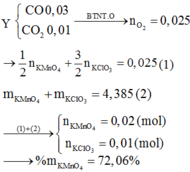
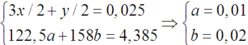
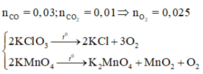
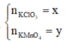
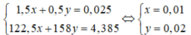
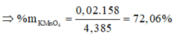


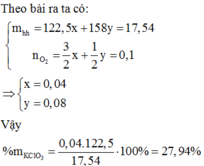
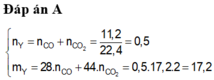
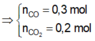
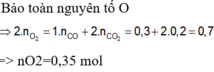
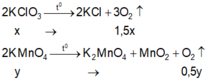
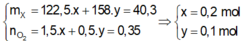



\(\overline{M}_Z=32\)
Gọi a là số mol của CO , b là số mol của CO2
\(\rightarrow a+b=\frac{0,896}{22,4}=0,04\left(mol\right)\left(1\right)\)
Ta có : \(\frac{28a+44b}{a+b}=32\)
\(\rightarrow4a=\frac{12b\Leftrightarrow a}{b}=3\Leftrightarrow a-3b=0\left(2\right)\)
Từ ( 1 ) và ( 2 ) \(\rightarrow\left\{{}\begin{matrix}a=0,03\\b=0,01\end{matrix}\right.\)
\(2C+O_2\underrightarrow{^{to}}2CO\)
\(C+O_2\underrightarrow{^{to}}CO_2\)
\(\Sigma n_{O2}=\frac{0,03}{2}+0,01=0,025\left(mol\right)\)
Gọi x là số mol của KClO3 , y là số mol của KMnO4
\(2KClO_3\rightarrow2KCl+3O_2\)
\(2KMnO_4\rightarrow K_2MnO_4+MnO_2+O_2\)
\(\rightarrow\left\{{}\begin{matrix}122,5x+158y=4,385\\1,5x+0,5y=0,025\end{matrix}\right.\rightarrow\left\{{}\begin{matrix}x=0,01\\y=0,02\end{matrix}\right.\)
\(\rightarrow m_{KClO_3}=1,225\left(g\right),m_{KMnO_4}=3,16\left(g\right)\)
Trong 8,77g X có 0,02 (mol) KClO3 , 0,04 (mol) KMnO4 ( x2 lượng X)
\(KClO_3+6HCl\rightarrow KCl+3Cl_2+3H_2O\)
\(KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\)
\(\Sigma n_{Cl2}=0,02.3+0,04.\frac{5}{2}=0,16\left(mol\right)\)
\(\rightarrow V_{Cl_2}=0,16.22,4=3,584\)