Đun nóng hỗn hợp X gồm 6 lít N2 và 12 lít H2 trong bình kín có xúc tác. Thể tích NH3 thu được là (biết hiệu suất của phản ứng 25%):
A. 48 lít.
B. 32 lít.
C. 3 lít.
D. 2 lít.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{hh}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
Do SO2 và O2 tỉ lệ mol 1:1
=> \(n_{SO_2}=n_{O_2}=0,2\left(mol\right)\)
\(2SO_2+O_2-^{t^o,V_2O_5}\rightarrow2SO_3\)
Lập tỉ lệ : \(\dfrac{0,2}{2}< \dfrac{0,2}{1}\) => Sau phản ứng O2 dư, tính theo số mol của SO2
Theo PT: \(n_{SO_3}=n_{SO_2}=0,2\left(mol\right)\)
Hỗn hợp khí Y gồm SO3, O2
\(SO_3+Ba\left(OH\right)_2\rightarrow BaSO_4\)
\(n_{BaSO_4}=n_{SO_3}=0,2\left(mol\right)\)
\(\Rightarrow m_{BaSO_{\text{4 }}\left(lt\right)}=0,2.233=46,6\left(g\right)\)
Thực tế chỉ thu được 45,8g kết tủa
\(\Rightarrow H=\dfrac{45,8}{46,6}=98,28\%\)

Đáp án B
Theo giả thiết, bảo toàn nguyên tố C và bảo toàn electron, ta có :
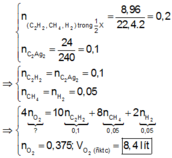

Chọn A.
Ta có: n Y = n H 2 = 0 , 04 m o l mol
=> E gồm các este của ancol (0,04) và các este của phenol (0,08 – 0,04 = 0,04)
mà n H 2 O = n este của phenol = 0,04 mol và n K O H = n este của ancol + 2neste của phenol = 0,12 mol
→ B T K L m E + m K O H = m muối + m ancol + m H 2 O Þ m muối = 13,7 gam
B