Hòa tan 8 gam 1 muối sunfat của một kim loại hóa trị 2 vào dung dịch NaOH dư sau phản ứng kết thúc thu được kết tủa lọc lấy kết tủa đem nung ở nhiệt độ cao thu được chất rắn là oxit dẫn lượng khí hidro qua oxit này nung nóng thì được 1 kim loại có khối lượng là 3,2 gam . Tìm kim loại từ đó tìm công thức của kim loại đó
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


ĐÁP ÁN B:
Do sắt dư nên phản ứng HNO3 chỉ tạo muối sắt 2
3Fe + 8H+ + 2NO3- ->3Fe2+ + 2NO + 4H2O
Mol 0,3 <- 0,8
Sơ đồ : Fe => Fe2+ => Fe(OH)2 => Fe2O3
Theo DLBT nguyrn tố Fe ta có => n Fe2O3 = ½ nFe = 0,15 mol => m rắn = m Fe2O3 = 24g
=> chọn B

Đáp án : B
VÌ có sắt dư nên chỉ tạo Fe2+
3Fe + 8H+ + 2NO3- -> 3Fe2+ + 2NO + 4H2O
=> nFe = 3/8nH+ = 0,3 mol = nFe2+
=> nFe2+ = nFe(OH)2 = 2nFe2O3
=> nFe2O3 = 0,15 mol => mrắn =24g

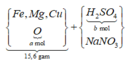
Đặt khối lượng kim loại trong hỗn hợp ban đầu là m gam; số mol O trong hoonx hợp ban đầu là a mol; số mol H2SO4 là b mol.
![]()
Sơ đồ phản ứng:
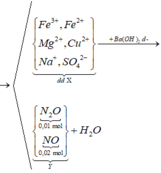
![]()
![]()
Các quá trình tham gia phản ứng của H+: 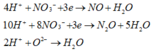
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
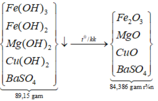
*Xét giai đoạn nung kết tủa đến khối lượng không đổi:
Sơ đồ phản ứng:
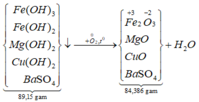
![]()
![]()
![]()
![]()
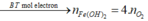
![]()
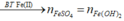
![]()
![]()
![]()
![]() = 85%.
= 85%.
Đáp án A.

Đáp án D
Tăng giảm khối lượng ta có
mO/MgO = 28 – 20 = 8 gam.
Bảo toàn nguyên tố Mg ta có
nMg = nMgO = 8 ÷ 16 = 0,5 mol.
⇒ nNO2 = 2nMg = 1 mol
Û VNO2 = 22,4 lít

Tăng giảm khối lượng ta có mO/MgO = 28 – 20 = 8 gam.
Bảo toàn nguyên tố Mg ta có nMg = nMgO = 8 ÷ 16 = 0,5 mol.
⇒ nNO2 = 2nMg = 1 mol Û VNO2 = 22,4 lít
Đáp án D





