Trong 1 loại nước ta thấy nồng độ Cl2 là 0,061M còn nồng độ của HCl và HClO là 0,03 M . Hỏi phải hòa tan bao nhiêu lít khí Cl2 ( đktc) vào nước để thu đc 5 lít nc Clo như trên.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


H2+Cl2->2HCl
0,35---0,7 mol
n H2=\(\dfrac{8,96}{22,4}\)=0,4 mol
n Cl2=\(\dfrac{7,84}{22,4}\)=0,35 mol
=>H2 dư :0,05 mol
=>VHCl=0,7.22,4=15,68l
b) C% HCl=\(\dfrac{0,7.36,5}{25,55+224,45}\).100=10,22%
a: \(H_2+Cl_2\rightarrow2HCl\)
\(n_{H_2}=\dfrac{8.96}{22.4}=0.4\left(mol\right)\)
\(n_{Cl_2}=\dfrac{7.84}{22.4}=0.35\left(mol\right)\)
=>Cl2 thiếu, H2 dư
\(V_{HCl}=2\cdot V_{Cl_2}=0.7\left(mol\right)\)

Đáp án A
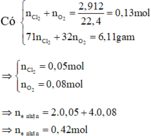
Y + HCl => Z chỉ chứa hai muối, HCl phản ứng hết
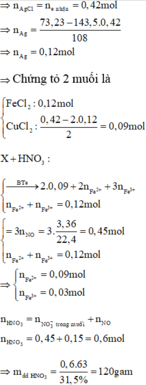
⇒ m dd T = 120 + 64 . 0 , 09 + 56 . 0 , 12 - 30 . 0 , 15 = 127 , 98 gam ⇒ C % Fe NO 3 3 = 242 . 0 , 03 127 , 98 . 100 % = 5 , 67 %
gần với giá trị 5% nhất

Câu 5:
\(n_{H_2}=\dfrac{0,896}{22,4}=0,04\left(mol\right)\)
PTHH: ACO3 + 2HCl --> ACl2 + CO2 + H2O
_____0,04<-----------------------0,04
=> \(M_{ACO_3}=\dfrac{4}{0,04}=100\left(g/mol\right)\)
=> MA 40 (g/mol)
=> A là Ca => CTHH của muối là CaCO3
Câu 6:
\(n_{Na_2O}=\dfrac{3,1}{62}=0,05\left(mol\right)\)
PTHH: Na2O + H2O --> 2NaOH
______0,05--------------->0,1
=> \(C_M=\dfrac{0,1}{0,2}=0,5M\)

Chọn B.
Hỗn hợp 5,8 gam có M (a mol) và M2Ox (b mol) Þ Ma + (2M + 16x).b = 5,8 (1)
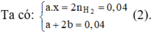
Với x = 1 hoặc 2 thay vào (1), (2) suy ra M = 137 (Ba)
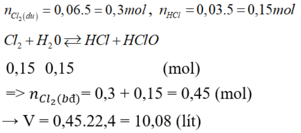


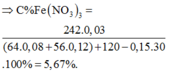
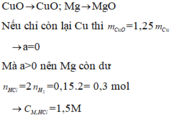

PTHH: \(H_2O+Cl_2\rightarrow HCl+HClO\\ 0,15:0,15\leftarrow0,15:0,15\)
\(n_{HCl}=n_{HClO}=0,03.5=0,15\left(mol\right)\)
\(n_{Cl_2trong5l}=0,061.5=0,305\left(mol\right)\)
\(V_{Cl_2candung}=\left(0,305+0,15\right).22,4=10,192\left(l\right)\)