Cho 19,1g hỗn hợp gồm Ba và Al phản ứng hoàn toàn với 6,72l hỗn hợp khí gồm Cl2 và O2 (đktc), thu được 36,5g hỗn hợp X gồm các muối và oxit. Hòa tan hoàn toàn hỗn hợp X vào dung dịch H2SO4 dư, thu được m(g) kết tủa. Tính giá trị của m.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án C
nMg=nFe=9,6/(24+56)=0,12 mol
nO=nH+/2=0,36/2=0,18 mol => nO2=0,09 mol
nCl2=z
Giả sử trong Y:
Fe2+: x
Fe3+: y
Cl-: 2z+0,36 (BTNT Cl)
Fe2+ + Ag+ → Fe3+ + Ag
x x
Ag+ + Cl- → AgCl
2z+0,36 2z+0,36
BTNT Fe: x+y=0,12 (1)
BT e: 0,12.2+2x+3y=2z+0,18.2 (2)
m kết tủa = 108x+143,5(2z+0,36) = 85,035 (3)
Giải hệ pt ta được: x=0,03; y=0,09; z=0,105
%VO2=0,09/(0,09+0,105)=46,15%

Đáp án D
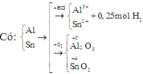
Vì trong hai thí nghiệm số oxi hóa của Sn trong sản phẩm thu được khác nhau nên ta cần tìm số mol cụ thể của mỗi kim loại trong hỗn hợp.
Một số bạn không để ý đến tính chất đặc biệt này của Sn mà cho rằng số oxi hóa của cả hai kim loại trong sản phẩm ở hai thí nghiệm là như nhau nên áp dụng ngay định luật bảo toàn mol electron:
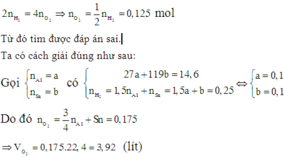

Đặt \(\left\{{}\begin{matrix}n_{Mg}=a\left(mol\right)\\n_{Fe}=b\left(mol\right)\\n_{Zn}=c\left(mol\right)\\n_{Al}=d\left(mol\right)\end{matrix}\right.\) \(\Rightarrow95a+127b+136c+133,5d=40,45\) (1)
Sau p/ứ với Clo, ta được: \(95a+162,5b+136c+133,5d=44\) (2)
Lấy PT (2) trừ PT (1) \(\Rightarrow35,5b=3,55\) \(\Rightarrow b=n_{Fe}=0,1\left(mol\right)\)
\(\Rightarrow\%m_{Fe}=\dfrac{0,1\cdot56}{13,47}\cdot100\%\approx41,57\%\)

\(n_{H^+} = n_{HCl} = 0,12.2 = 0,24(mol)\\ 2H^+ + O^{2-} \to H_2O\\ n_{O(oxit)} = \dfrac{1}{2}n_{H^+} = 0,12(mol)\\ \Rightarrow n_{O_2} = \dfrac{n_{O(oxit)}}{2} = 0,06(mol)\\ n_{Mg} = \dfrac{1,68}{24} = 0,07(mol) ; n_{Al} = \dfrac{2,16}{27} = 0,08(mol)\)
Bảo toàn electron :
\(2n_{Mg} + 3n_{Al} = 4n_{O_2} + 2n_{Cl_2}\\ \Rightarrow n_{Cl_2} = \dfrac{0,07.2 + 0,08.3-0,06.4}{2} = 0,07(mol)\\ \Rightarrow \%V_{Cl_2} = \dfrac{0,07}{0,07+0,06}.100\% = 53,85\%\)

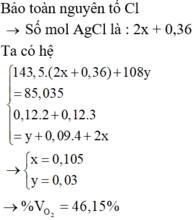




Gọi số mol O2 là a Cl2 là b
Ta có\(\left\{{}\begin{matrix}\text{32a+71b=36,5-19,1=17,4}\\\text{a+b=0,3}\end{matrix}\right.\rightarrow\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
Gọi số mol Ba là x số mol Al là y
Bảo toàn e ta có\(\left\{{}\begin{matrix}\text{2x+3y=4a+2b=0,8}\\\text{137x+27y=19,1}\end{matrix}\right.\rightarrow\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
\(\rightarrow\)m=mBaSO4=0,1.233=23,3(g)
Bạn g/thích cho mình chỗ 2x+3y = 4a+2b đc k z??? Mình chưa hiểu chỗ này cho lắm!!!