Hòa tan hỗn hợp A gồm kim loại R(chỉ có có trị II) và muối cacbonat của R trong 80 ml dung dịch HNO3 1M thì thu được dung dịch B chỉ chứa một muối và hỗn hợp 2 khí có khối lượng mol trung bình là 45,5 g/mol. Cho B tác dụng với dung dịch NaOH dư rồi nung kết tủa tạo ra đến khối lượng không đổi được 1 gam chất rắn.
A) Xác định kim loại R
b) Tính thành phần % về khối lượng trong hỗn hợp A
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án A.
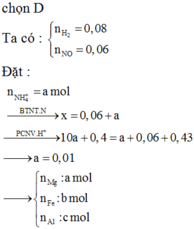
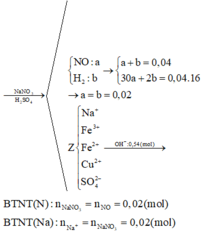
Hỗn hợp khí gồm H2 và NO.
⇒ n H 2 + n N O = 0 , 896 22 , 4 = 0 , 04 m o l 2 n H 2 + 30 n N O = 0 , 04 . 8 . 2 = 0 , 64 g
⇒ n H 2 = 0 , 02 m o l n N O = 0 , 02 m o l
→ B T N T N n N a N O 3 = n N O = 0 , 02 m o l
· Z + 0,54 mol NaOH:
→ B T N T N a n N a 2 S O 4 = 0 , 28 m o l
⇒ n H 2 S O 4 = 0 , 28 m o l
⇒ m X = 11 , 92 gam
n H + = 3 n N O + 3 n H 2 + n N O + 2 n O = 0 , 56 m o l
⇒ n O = 0 , 56 - 4 . 0 , 02 - 2 . 0 , 02 2 = 0 , 22 m o l
⇒ m = 15 , 44 gam






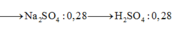
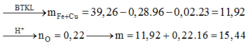
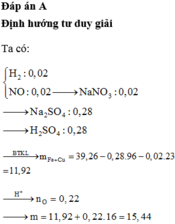
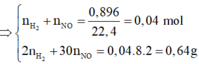
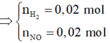
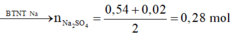
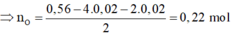


a)
Ta có Mhh=45,5(g/mol)
\(\rightarrow\)Khí là CO2 và NO2
R+4HNO3\(\rightarrow\)R(NO3)2+2NO2+2H2O
RCO3+2HNO3\(\rightarrow\)R(NO3)2+CO2+H2O
R(NO3)2+2NaOH\(\rightarrow\)R(OH)2+NaNO3
R(OH)2\(\rightarrow\)RO+H2O
Ta có
Theo pp đường chéo ta có
Gọi a là số mol CO2\(\rightarrow\)nNO=3a
Ta có\(\text{ 2a+6a=0,08}\)\(\rightarrow\)a=0,01(mol)
\(\Rightarrow\)nR(NO3)2=\(\frac{0,03}{2}\)+0,01=0,025(mol)
\(\Rightarrow\)nRO=0,025(mol)
\(\Rightarrow\)MRO=40
\(\Rightarrow\)MR=24(đVC)
\(\Rightarrow\)R là Mg
b)
\(\text{mMg=0,015.24=0,36(g)}\)
mMgCO3=0,01.84=0,84(g)
%Mg=\(\frac{\text{0,36}}{\text{0,36+0,84}}\).100=30%
\(\Rightarrow\text{%MgCO3=100-30=70%}\)
thank you