Xác định khối lượng của muối kali clorua kết tinh được sau khi làm nguội 604g dung dịch bão hòa ở 800C xuống 200C. Độ tan của KCl ở 800C bằng 51g ở 200C là 34g.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Ở 80oC: 51(g) KCl + 100(g) H2O => 151(g) dung dịch KCl bào hòa
=> x (g) KCl + y (g) H2O ==> 604 (g) dung dịch KCl bão hòa
=> \(\left\{\begin{matrix}x=\frac{604\times51}{151}=204\left(g\right)\\y=\frac{604\times100}{151}=400\left(g\right)\end{matrix}\right.\)
Ở 20oC: 34(g) KCl + 100(g) H2O => Dung dịch bão hòa
=> a (gam) KCl + 400 (g) H2O => Dung dịch bão hòa
=> a = \(\frac{400\times34}{100}=136\left(gam\right)\)
=> Khối lượng KCl kết tinh: 204 - 136 = 68 (gam)

Từ 80oC -> 20oC chất tan tan trong dung dịch giảm :
\(\Delta_S=51-34=17\)
151g dd bão hòa từ 80oC -> 20oC có khối lượng kết tinh là 17g
604g dd bão hòa từ 80oC -> 20oC có khối lượng kết tinh là x
\(\Rightarrow x=\dfrac{604.17}{151}=68\left(g\right)\)

Bài 1 :
Khối lượng KCl trong ddbh ở t1 = 800 độ C là :
mKCl(1) = \(\frac{51}{100+51}.604=204\left(g\right)\)
Khối lượng nước ở t1 là
mH2O = \(\frac{100}{100+51}.604=400\left(g\right)\)
Khối lượng kcl trong ddbh ở t2 = 200 độ C là
mKCl(2) = \(\frac{34}{100}.400=136\left(g\right)\)
Khối lượng KCl kết tinh là :
mKCl (kt) = mKCl(1) - mKCl(2) = 204 - 136 = 68(g)
Cách khác :
mKCl(kt) = \(\frac{\left(51-34\right).604}{100+51}=68\left(g\right)\)

Gọi khối lượng KCl trong dd bão hòa ở 80oC là a (g)
\(S_{80^oC}=\dfrac{a}{604-a}.100=51\left(g\right)\)
=> a = 204 (g)
=> mH2O = 604 - 204 = 400 (g)
Gọi khối lượng KCl trong dd bão hòa ở 20oC là b (g)
\(S_{20^oC}=\dfrac{b}{400}.100=34\left(g\right)\)
=> b = 136 (g)
mKCl(kết tính) = a - b = 68 (g)
Ở 80 độ C :
Cứ 51 (g) KCl tan trong 151 (g) dung dịch KCl
=> Cứ 204 (g) KCl tan trong 604 (g) dung dịch KCl
mH2O (80 độ C) = 604 - 204 = 400 (g)
Làm lạnh dung dịch => Lượng nước trong dung dịch không đổi
=> mH2O (20 độ C) = 400 (g)
* Ở 20 độ C:
Cứ 34 (g) KCl tan tối đa trong 100 (g) nước
=> Cứ 136 (g) KCl tan tối đa trong 400 (g) nước
=> mKCl tách = 204 - 136 = 68 (g)


[LỜI GIẢI] Giả thiết độ tan của CuSO4 ở 100C và 800C lần lượt là 17,4 gam và 55 g - Tự Học 365 Nguồn ở đây nha

100g H 2 O ở 20 0 C hòa tan được 34g KCl
130g H 2 O ở 20 0 C hòa tan được x?g KCl
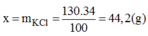

- Ở 80oC, độ tan của KCl là 51 gam:
151 gam dung dịch bão hòa chứa 51 gam KCl
=> 604 gam.................→....................204 gam
Đặt khối lượng KCl tách ra là m gam
- Ở 20oC, độ tan của KCl là 34 gam:
134 gam dung dịch bão hòa chứa 34 gam KCl
604-m gam.......................................204-m gam
=> 34.(604 - m) = 134.(204 - m) => m = 68 gam
Vậy khối lượng KCl kết tinh được là 68 gam.
Ở 80oC: 51g KCl + 100gH2O => 151g dung dịch KCl bào hòa
=> x g KCl + y g H2O ==> 604 g dung dịch KCl bão hòa
-->x=\(\frac{604.51}{151}=204\left(g\right)\)
-->y=\(\frac{604.100}{151}=400\left(g\right)\)
=> Ở 20oC: 34g KCl + 100g H2O => Dung dịch bão hòa
=> a gKCl + 400 g H2O => Dung dịch bão hòa
=> a = 400×34/100=136(g)
=> Khối lượng KCl kết tinh: 204 - 136 = 68 (gam)