Cho hổn hợp hai kim loại kiềm kế tiếp nhau tác dụng với nước , thu được dd X và 36ml khi hidro ở (đktc) cho dd X tác dụng HCl thu được 2,075g
a, tìm kim loại
b, tìm % khối lượng mỗi kim loại
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi kim loại kiềm thổ chung là R.
\(R+2HCl\rightarrow RCl_2+H_2\)
0,25 0,25
\(\Rightarrow M_R=\dfrac{8,15}{0,25}=32,6\)
\(\Rightarrow R_1< 32,6< R_2\)
Mà hai kim loại nằm ở 2 chu kì liên tiếp nên:
\(\left\{{}\begin{matrix}R_1:24\left(Mg\right)\\R_2:40\left(Ca\right)\end{matrix}\right.\)

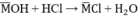
Theo pt: nHCl = nMOH = 0,1 (mol)
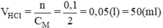
m(MCl) = 0,1.(31 + 35,5) = 6,65(g)

Gọi công thức chung của 2 kim loại là A
\(n_{H_2}=\dfrac{0,896}{22,4}=0,04\left(mol\right)\)
PTHH: 2A + 2H2O --> 2AOH + H2
_____0,08<-----------------------0,04
=> \(\overline{M}_A=\dfrac{1,28}{0,08}=16\left(g/mol\right)\)
=> 2 kim loại đó là Li và Na

a, Đặt kim loại trung bình là R \(\rightarrow \) R hóa trị II
\(PTHH:R+2HCl\to RCl_2+H_2\\ \Rightarrow n_R=n_{H_2}=\dfrac{4,48}{22,4}=0,2(mol)\\ \Rightarrow M_R=\dfrac{6,5}{0,2}=32,5(g/mol)\)
Vậy 2 KL đó là Mg (24) và Ca (40)
\(b,\) Đặt \((n_{Mg};n_{Ca})=(x;y)(mol)\)
\(\Rightarrow \begin{cases} 24x+40y=6,5\\ x+y=n_{H_2}=0,2 \end{cases}\Rightarrow \begin{cases} x=0,09375(mol)\\ y=0,10625(mol) \end{cases}\\ \Rightarrow \begin{cases} m_{Mg}=2,25(g)\\ m_{Ca}=4,25(g) \end{cases}\)

Đáp án A
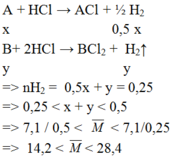
Chỉ có cặp nghiệm A = 23 (Na ) , B = 24 (Mg) thỏa mãn

Gọi CTTQ hai kim loại là R
Gọi $n_{H_2} = a(mol)$
$R + 2HCl \to RCl_2 + H_2$
Theo PTHH :
Ta có :
$Ra - 2a = 0,82$
$a(R + 71) = 1,915$
Suy ra : a = 0,015 ; Ra = 0,85
$m_{hai\ kim\ loại} = Ra = 0,85(gam)$
$\Rightarrow R = \dfrac{0,85}{0,015} = 56,67$
Vậy hai kim loại là Canxi và Stronti

Gọi công thức chung cho hai kim loại kiềm là M
Số mol H2: nH2 = 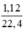 = 0,05(mol)
= 0,05(mol)
PTHH: 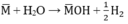
Theo pt: nM = 2. nH2 = 2. 0,05 = 0,1(mol)
⇒ M = 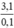 = 31 → Na, K
= 31 → Na, K
Gọi x, y lần lượt là số mol của Na và K trong hỗn hợp
Theo bài ra ta có hệ phương trình:
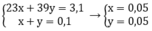
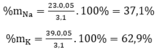

a) Gọi công thức chung của 2 kim loại kiềm là M
2M + 2H2O → 2MOH + H2
nH2nH2 = 0,05 mol ⇒ nM= 2nH2 =0,1 mol
⇒ M = 3,1/0,1= 31 (g/mol); Vậy 2 kim loại đó là Na (23) và K (39)
Gọi x là số mol kim loại Na, ⇒ nK = 0,1 – x (mol)
ta có: m hỗn hợp = mNa + mK
⇔ 3,1 = 23x + 39(0,1 - x)
⇒ x = 0,05 mol
%mNa=mNa/mhh*100%=23*0,05/3,1*100%*100%= 37,1%;
% mK = 100% - 37,1% = 62,9%.
b) HCl + MOH → MCl + H2O
nHCl =nMOH = 0,1 mol ⇒Vdung dịch HCl = n/CM=0,1/2=0,05lítnCM=0,12=0,05lí
mhh muối= mKL + mCl= 3,1 + 35,5.0,1= 6,65 (gam)
a. Gọi công thức chung cho hai kim loại kiềm là M
Số mol H2: nH2 = 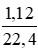
PTHH:
Theo pt: nM = 2. nH2 = 2. 0,05 = 0,1(mol)
⇒ M = 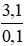
Gọi x, y lần lượt là số mol của Na và K trong hỗn hợp
Theo bài ra ta có hệ phương trình:
b.
Theo pt: nHCl = nMOH = 0,1 (mol)
m(MCl) = 0,1.(31 + 35,5) = 6,65(g)
Sửa đề : 336 ml
Gọi: 2 kim loại là : M
nH2 = 0.015 mol
M + H2O --> MOH + 1/2H2
____________0.03____0.015
MOH + HCl --> MCl + H2O
0.03__________0.03
M = 2.075/0.03 =69.17
<=> M + 35.5 = 69.17
=> M = 33.67
Kim loại cần tìm là : K và Na
% bạn tự gọi số mol và giải phương trình nhé
Tham khảo!