Khử hoàn toàn 2,4 hỗn hợp CuO và oxit sắt bằng hidro dư đun nóng sau phản ứng thu được 1,76 g chất rắn hòa tan rắn vừa thu được bằng dung dịch axit HCL dư khi phản ứng kết thúc phản ứng thu được 0,448 lít hidro ở điều kiện tiêu chuẩn xác định công thức phân tử của oxit sắt
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



khử hoàn toàn 24 g hoá học CuO và oxit sắt bằng hidro dư đun nóng .sau phản ứng thu được 1,76 g chất rắn . hoà tan chất rắn vừa thu được bằng dung dịch axit HCl dư.khi phản ứng kết thúc thu được 0,448 l khí H2 ở điều kiện tiêu chuẩn
a)xác định công thức phân tử oxit sắt

1.Đưa que đóm đang cháy vào 4 chất khí: O2 bùng cháy sáng
Còn lại 3 chất khí CO,CO2,H2
Sục 3 chất khí vào dd \(Ca\left(OH\right)_2\)
-CO2: xuất hiện kết tủa trắng
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3\downarrow+H_2O\)
-H2,CO: không hiện tượng
Đưa 2 chất khí đi qua CuO ở nhiệt độ thích hợp và Ca(OH)2
-CO2: kết tủa trắng
-H2: không hiện tượng
\(CuO+CO\rightarrow\left(t^o\right)Cu+CO_2\)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3\downarrow+H_2O\)
\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2\)
2.
\(n_{H_2}=\dfrac{0,448}{22,4}=0,02mol\)
\(Fe+HCl\rightarrow FeCl_2+H_2\)
0,02 0,02 ( mol )
\(m_{Fe}=0,02.56=1,12g\)
\(\Rightarrow m_{Cu}=1,76-1,12=0,64g\)
\(n_{Cu}=\dfrac{0,64}{64}=0,01mol\)
\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\)
0,01 0,01 ( mol )
\(m_{CuO}=0,01.80=0,8g\)
\(\Rightarrow m_{Fe_xO_y}=2,4-0,8=1,6g\)
\(Fe_xO_y+yH_2\rightarrow\left(t^o\right)xFe+yH_2O\)
\(\dfrac{1,6}{56x+16y}\) -----> \(\dfrac{1,6x}{56x+16y}\) ( mol )
Ta có:
\(\dfrac{1,6x}{56x+16y}=0,02\)
\(\Leftrightarrow1,6x=1,12x+0,32y\)
\(\Leftrightarrow3x=2y\)
\(\Leftrightarrow x=2;y=3\)
\(\Rightarrow CTHH:Fe_2O_3\)
\(\%m_{Fe_2O_3}=\dfrac{1,6}{2,4}.100=66,67\%\)
\(\%m_{CuO}=100\%-66,67\%=33,33\%\)

a) A gồm Cu, Fe
\(n_O=\dfrac{39,2-29,6}{16}=0,6\left(mol\right)\)
=> \(n_{H_2O}=0,6\left(mol\right)\)
=> \(n_{H_2}=0,6\left(mol\right)\)
=> \(V_{H_2}=0,6.22,4=13,44\left(l\right)\)
b)
Gọi \(\left\{{}\begin{matrix}n_{CuO}=a\left(mol\right)\\n_{Fe_xO_y}=b\left(mol\right)\end{matrix}\right.\)
=> 80a + b(56x + 16y) = 39,2
=> 80a + 56bx + 16by = 39,2 (1)
nO = 0,6 (mol)
=> a + by = 0,6
=> 80a + 80by = 48 (2)
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
0,3<-------------------0,3
=> nFe = bx = 0,3 (mol)
(2) - (1) => 64by - 56bx = 8,8
=> by = 0,4
Xét \(\dfrac{bx}{by}=\dfrac{x}{y}=\dfrac{0,3}{0,4}=\dfrac{3}{4}\)
=> CTHH: Fe3O4
Có: \(\left\{{}\begin{matrix}80a+232b=39,2\\a+4b=0,6\end{matrix}\right.\)
=> a = 0,2; b = 0,1
=> \(\left\{{}\begin{matrix}m_{CuO}=0,2.80=16\left(g\right)\\m_{Fe_3O_4}=0,1.232=23,2\left(g\right)\end{matrix}\right.\)

nHCl cần = 2nO trong oxit = 0,24 mol → nHCl đã dùng (dư 25%) = 0,3 mol.
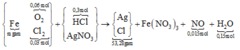
Ghép cụm có nH2O = nO trong oxit + 2nNO
→ nNO = 0,015 mol.
∑nCl = 0,36 mol đi hết vào 53,28 gam tủa
→ về nguyên tố nAg trong tủa = 0,375 mol
Bảo toàn N có nFe(NO3)3 = (0,375 – 0,015) ÷ 3 = 0,12 mol.
→ Yêu cầu m = mFe = 0,12 × 56 = 6,72 gam.
Đáp án A

Đáp án A
Ta có nHCl cần dùng = 2∑nO trong oxit = 0,24 mol → ∑nHCl đã dùng (dư 25%) = 0,3 mol.
* Gộp cả quá trình có sơ đồ:
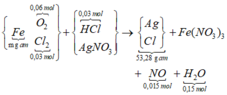
Ghép cụm NO3 bảo toàn O hoặc bảo toàn electron mở rộng ta có:
![]()
∑nCl = 0,36 mol đi hết vào 53,28 gam tủa → về mặt nguyên tố ∑nAg trong tủa = 0,375 mol.
→ Bảo toàn nguyên tố N có
![]()
Theo đó, m gam Fe ban đầu tương ứng với 0,12 mol → m = 0,12 × 56 = 6,72 gam.


