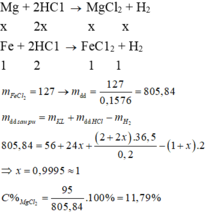Hòa tan hoàn toàn hỗn hợp X gồm Fe và Mg bằng 1 lượng vừa đủ dd HCl 20% thu được dd Y. C% FeCl2 trong dd Y là 15,76%. Tính C% MgCl2 trong dd Y
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Fe + 2HCl => FeCl2 + H2 (1)
Mg + 2HCl => MgCl2 + H2 (2)
=> Y : FeCl2 , MgCl2
Giả sử nHCl = 1(mol),nFe = a (mol),nMg = b (mol)
=> mdd HCl = \(\frac{1.36,5}{20\%}=182,5\left(g\right)\)
mX = mFe + mMg = 56.a + 24.b (g)
(1),(2) => nH2 = nFe + nMg = a+b (mol)
=> mH2 = 2.(a+b) (g)
(1),(2) => nHCl = 2.(nFe + nMg) = 2.(a+b )(mol)
=> 2.(a+b) = 1 => a+b= 0,5
mY = mX + mdd HCl - mH2
= 56.a+24.b+182,5-2(a+b)
= 32.a+193,5 (g)
%mFeCl2 = 15,76%
=> \(\frac{127.a}{32.a+193,5}.100\%=15,76\%\)
=> a = 0,25
=> b = 0,25
=> mMgCl2 = 0,25.95 = 23,75 (g)
mY = 32.0,25+193,5 = 201,5 (g)
=> %mMgCl2 = \(\frac{23,75}{201,5}.100\%=11,79\%\)

a, PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
b, Gọi: \(\left\{{}\begin{matrix}n_{Fe}=x\left(mol\right)\\n_{Mg}=y\left(mol\right)\end{matrix}\right.\)
Theo PT: \(\left\{{}\begin{matrix}n_{HCl}=2n_{Fe}+2n_{Mg}=2x+2y\left(mol\right)\\n_{H_2}=n_{Fe}+n_{Mg}=x+y\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m_{HCl}=36,5.\left(2x+2y\right)=73\left(x+y\right)\left(g\right)\)
\(\Rightarrow m_{ddHCl}=\dfrac{73\left(x+y\right)}{20\%}=365\left(x+y\right)\left(g\right)\)
Ta có: m dd sau pư = mFe + mMg + m dd HCl - mH2 = 56x + 24y + 365.(x+y) - 2.(x+y) = 419x + 387y (g)
Theo PT: \(n_{MgCl_2}=n_{Mg}=y\left(mol\right)\)
\(C\%_{MgCl_2}=11,87\%\) \(\Rightarrow\dfrac{95y}{419x+387y}=0,1187\)
\(\Rightarrow\dfrac{x}{y}=0,9865\Rightarrow x=0,9865y\)
Theo PT: \(n_{FeCl_2}=n_{Fe}=x\left(mol\right)\)
\(\Rightarrow C\%_{FeCl_2}=\dfrac{127x}{419x+387y}.100\%=\dfrac{127.0,9865y}{419.0,9865y+387y}.100\%\approx15,65\%\)

Chọn đáp án B
L ấ y 1 m o l F e : x m o l M g : x - 1 m o l
F e + 2 H C l → F e C l 2 + H 2 ↑ x 2 x x x
M g + 2 H C l → M g C l 2 + H 2 ↑ 1 - x 2 1 - x 1 - x 1 - x
n H 2 = 1 m o l , n H C l = 2 m o l ⇒ m d d H C l = 2 . 36 , 5 . 100 20 = 365 g m d d Y = 56 x + 24 1 - x + 365 - 1 . 2 = 387 + 32 x
C % F e C l 2 = 127 x 387 + 32 x . 100 % = 15 , 76 % ⇒ x = 0 , 5 m o l ⇒ C % M g C l 2 = 95 . 0 , 5 387 + 32 . 0 , 5 . 100 % = 11 , 79 %

1.GS có 100g dd $HCl$
=>m$HCl$=100.20%=20g
=>n$HCl$=20/36,5=40/73 mol
=>n$H2$=20/73 mol
Gọi n$Fe$(X)=a mol n$Mg$(X)=b mol
=>n$HCl$=2a+2b=40/73
mdd sau pứ=56a+24b+100-40/73=56a+24b+99,452gam
m$MgCl2$=95b gam
C% dd $MgCl2$=11,79%=>95b=11,79%(56a+24b+99,452)
=>92,17b-6,6024a=11,725
=>a=0,13695 mol và b=0,137 mol
=>C%dd $FeCl2$=127.0,13695/mdd.100%=15,753%
2.Bảo toàn klg=>mhh khí bđ=m$C2H2$+m$H2$
=0,045.26+0,1.2=1,37 gam
mC=mA-mbình tăng=1,37-0,41=0,96 gam
HH khí C gồm $H2$ dư và $C2H6$ không bị hấp thụ bởi dd $Br2$ gọi số mol lần lượt là a và b mol
Mhh khí=8.2=16 g/mol
mhh khí=0,96=2a+30b
nhh khí=0,06=a+b
=>a=b=0,03 mol
Vậy n$H2$=n$C2H6$=0,03 mol

Đáp án B
Fe+2HCl → FeCl2 + H2
a 2a a a
Mg + 2HCl → MgCl2+H2
b 2b b b
mchất rắn X = 56a + 24b ; mddHCl = 36,5/20% .2.(a + b) = 365(a + b)
![]()
⇒ mddsau pư = 56a + 24b + 365(a + b) – 2(a + b) = 419a + 387b
![]() .100 = 15,76
.100 = 15,76
Giải PT ⇒ a = b ⇒ ![]() .100 = 11,79%
.100 = 11,79%

Gọi nFe= x (mol); nMg= y(mol)
PTHH: Fe +2 HCl \(\rightarrow\) FeCl2 + H2\(\uparrow\)
x-> 2x x x (mol)
Mg + 2HCl \(\rightarrow\) MgCl2 + H2\(\uparrow\)
y-> 2y y y (mol)
Ta có: mdd sau p.ứng = \(56x+24y+\frac{\left(73x+73y\right).100}{20}-\left(2x+2y\right)\)
= 419x + 387y (g)
mFeCl2 = 127x (g)
\(\Rightarrow\) C%FeCl2 = \(\frac{127x}{419x+387y}.100\) = 15,76%
\(\Leftrightarrow\) \(\frac{127x}{419x+387y}\) = 0,1576
\(\Leftrightarrow\) \(\frac{x}{y}=1\) \(\Leftrightarrow\) x=y
Ta có: mMgCl2 = 95y = 95x(g)
m dd sau p.ứng = 419x + 387y = 419x + 387x = 806x (g)
\(\Rightarrow\) C% MgCl2 = \(\frac{95x}{806x}.100\) = 11,79%