Cho m gam Mg tác dụng vừa đủ với 200ml dung dịch CH3COOH !M. Sau phản ứng thu được dung dịch a và V lít khí ở đktc
a, tính m và V
b, cần lên men bao nhiêu ml dụng dịch rượu etylic 8 độ để thu được axit axetic đủ tham gia phản ứng với Mg ở trên? Biết hiieuj suất phản ứng là 100% D rượu etylic=0,8g/ml

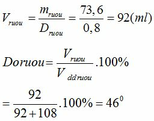
Phương trình hóa học:
Mg + 2CH3COOH => (CH3COO)2Mg + H2
nCH3COOH = CM.V = 0.2 x 1 = 0.2 (mol)
Theo phương trình ==> nMg = 0.1 (mol) => mMg = n.M = 0.1 x 24 = 2.4 (g)
Theo phương trình ==> nH2 = 0.1 (mol) ==> VH2 =22.4 x n = 22.4 x 0.1 = 2.24 (l)
C2H5OH + O2 => (men giấm) CH3COOH + H2O
nCH3COOH = 0.2 (mol) => nC2H5OH = 0.2 (mol)
mC2H5OH = n.M = 0.2 x 46 = 9.2 (g)
V = m/D = 9.2/8 = 1.15ml
nCH3COOH= 0.2 mol
Mg + 2CH3COOH --> (CH3COO)2Mg + H2
Từ PTHH:
nMg= 0.1 mol
mMg=2.4g
nH2= 0.1 mol
VH2= 2.24l
C2H5OH + O2 -mg-> CH3COOH + H2O
0.2___________________0.2
mC2H5OH= 9.2g
VC2H5OH=9.2/0.8=11.5ml
V hhr= 11.5*100/8=143.75ml