1.Cho m gam Mg vào dd chứa 0,3 mol fe(no3)3 và 0,71 mol cu(no3)2, sau một thời gian thu được (m+28) g kim loại. khối lượng Mg pư là : A.23,04 B.16,56 C.27,84 D.22,08
2.Cho 8,64 g Al vào dd X ( được tạo thành bằng cách hòa tan 74,7 g hỡn hợp Y gồm CuCl2 và FeCl3 vào nước). kết thúc pư thu được 17,76 g chất rắn gồm hai kim loại. tỉ lệ số mol fecl3 : cucl2 trong hỗn hợp Y là : A.2:1 B.3:2 C.3:1 D.5:3
3.Cho một thanh sắt có khối lượng m gam vào dd chứa 0,012 mol agno3 và 0,02 mol cu(no3)2, sau một thời gian khối lượng thanh săt là (m+14) g kim loại. Tính khối lượng của kim loại bám trên sắt : A.2,576 B.1,296 C.0,896 D.1,936
4.Nhúng thanh Fe vào 200mol dd fecl3 x (mol/l) và cucl2 y (mol/l). sau khi kết thúc phản ứng lấy thanh fe ra lau khô cẩn thận, cân lại thấy khôi lượng ko đổi so với trước pư. biết lượng Cu sinh ra bám hoàn toàn vào thanh Fe. tỉ lệ x:y
A.3:4 B. 1:7 C.2:7 D.4:5
5. Cho m g bột Fe vào dd X chứa agno3 và cu(no3)2 đến khi các pư kết thúc thu được cr Y và dd Z. cho dd Z tác dụng hết với dd NaOH dư, thu được a(g) kết tủa T gồm 2 hidroxit kim loại Nung T đến khối lượng ko đổi thu được b g cr. biểu thức liên hệ giữa m,a,b có thể là: A.m=8,225b-7a B.m=8,575b-7a C.m=8,4b-3a D. m=9b-6,5a



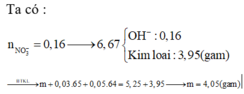
Bài 5:
\(\underrightarrow{BT:Fe}n_{Fe}=n_{Fe\left(OH\right)_2}=\dfrac{m}{56}\left(mol\right)\)
\(\rightarrow n_{Fe_2O_3}=\dfrac{m}{112}\left(mol\right)\rightarrow m_{Fe\left(OH\right)_2}=\dfrac{45}{28}m\left(gam\right)\)
mà \(m_{Fe_2O_3}+m_{CuO}=b\rightarrow m_{CuO}=\left(b-\dfrac{10}{7}m\right)gam\)
\(\underrightarrow{BT:Cu}m_{Cu\left(OH\right)_2}=\left(\dfrac{49b-70m}{40}\right)gam\)
Ta có: \(m_{Fe\left(OH\right)_2}+m_{Cu\left(OH\right)_2}=a\rightarrow\dfrac{45m}{28}+\dfrac{49b-70m}{40}\)
\(\rightarrow m=8,575b-7a\)
Vậy chọn đáp án B
Bài 2:
Bảo toàn khối lượng, ta có: \(133,5_{n_{AlCl_3}}+127_{n_{FeCl_2}}=m_{Al}+m_Y-m_{ran}=65,68\left(g\right)\)
Bảo toàn nguyên tố: \(n_{AlCl_3}=n_{Al}=0,32\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{AlCl_3}=0,32\left(mol\right)\\n_{FeCl_2}=0,18\left(mol\right)\end{matrix}\right.\)
Trong Y có: \(\left\{{}\begin{matrix}133,5_{n_{CuCl_2}}=+162,5_{n_{FeCl_3}}=m_Y=74,7\\2n_{CuCl_2}+3n_{FeCl_3}=3n_{AlCl_3}+2n_{FeCl_2}=1,32\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}n_{FeCl_3}=0,36\left(mol\right)\\n_{CuCl_2}=0,12\left(mol\right)\end{matrix}\right.\) Suy ra tỉ lệ là 3:1
Vậy chọn đáp án C
Bài 3:
Bài 4: