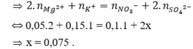Dung dịch X chứa 0,15 mol Mg2+ , 0,15 mol Al3+ ; 0,9 mol Cl và a mol Cu2+ Cho 650 ml dung dịch NaOH 1,5M vào X , khuấy đều cho các phản ứng xảy ra hoàn toàn , thu được khối lượng kết tủa là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Giải thích:
BTĐT: nHCO3-=0,1.2+0,15-0,15=0,2 mol
Coi như A chỉ có Mg(HCO3)2, để x đạt giá trị tối thiểu:
Mg(HCO3)2+Ca(OH)2→CaCO3+MgCO3+H2O
=>x=0,1 mol
Đáp án A

Đáp án B
Loại ngay A và D do H+ và CO32- không tồn tại trong cùng 1 dung dịch
Xét B: nK+ + nNH4+ = 0,15 + 0,25 = 0,4 mol; nCl- + 2nCO32- = 0,1 + 2.0,15 = 0,4 mol
=> thỏa mãn định luật bảo toàn điện tích
Xét C: nK+ + 2nMg2+ = 0,15 + 2.0,1 = 0,35 mol; nCl- + 2nSO42- = 0,1 + 2.0,075 = 0,25 mol
=> không thỏa mãn định luật bảo toàn điện tích

Chọn A
Bảo toàn điện tích : nNa+ + 2nMg2+ + 2nCa2+ = nHCO3 + nCl
=> x = 0,35 mol

Đáp án B
Bảo toàn điện tích, ta có: 0,05.2 + 0,15 = 0,1 + 2x => x = 0,075 => Chọn B.

Bảo toàn điện tích → 0,05.2 + 0,15.1 = 0,1.1 + 2x → x = 0,075
Đáp án B

Đáp án B
Bảo toàn điện tích => 0,05.2 + 0,15.1 = 0,1.1 + 2x => x = 0,075

Đáp án B
Áp dụng định luật bảo toàn điện tích: tổng số mol điện tích dương bằng tổng số mol điện tích âm
nên 2.0,05+ 0,15.1= 0,1.1+ 2x → x= 0,075 mol

Bảo toàn điện tích → 0,05.2 + 0,15.1 = 0,1.1 + 2x → x = 0,075
Đáp án B

Đáp án B
Bảo toàn điện tích, ta có: 0,05.2 + 0,15 = 0,1 + 2x => x = 0,075