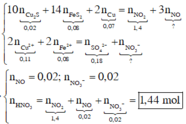Cho 12,8 gam Cu hòa tan trong m gam dd HNO3 12,6% vừa đủ. Sau phản ứng thu được V lít khí NO là sản phẩm khử duy nhất ở đktc và dung dịch A. Tính m, V và tính nồng độ phần trăm chất tan có trong A.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a)
\(n_{NO} = 0,01(mol)\)
Bảo toàn electron : \(2n_{Cu} = 3n_{NO}\)
\(\Rightarrow n_{Cu} = 0,015(mol)\)
Vậy :
\(\%m_{Cu} = \dfrac{0,01.64}{1,98}.100\% = 32,32\%\\ \%m_{Al_2O_3} = 100\% - 32,32\% = 67,68\%\)
b)
\(n_{Al_2O_3} = \dfrac{1,98-0,015.64}{102} = 0,01(mol)\)
\(n_{OH^-} = n_{NaOH} + 2n_{Ba(OH)_2} = 0,1.1 + 0,5.0,1.2 = 0,2(mol)\)
Ta có :
\(n_{Cu(NO_3)_2} = n_{Cu} = 0,015(mol)\\ n_{Al(NO_3)_3} = 2n_{Al_2O_3} = 0,02(mol)\)
Mà : \(n_{OH^-} = 4n_{Al(NO_3)_3} + 2n_{Cu(NO_3)_2} + n_{HNO_3\ dư}\)
\(\Rightarrow n_{HNO_3\ dư} = 0,09(mol)\)
Bảo toàn nguyên tố với N :
\(n_{HNO_3\ pư} = 3n_{Al(NO_3)_3} + 2n_{Cu(NO_3)_2} = 0,06(mol)\)
Vậy, \(V = \dfrac{0,09 + 0,06}{1} = 0,15(lít)\)

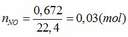
Fe + 4HNO3 → Fe(NO3)3 + NO + 2H2O (1)
a → 4a → a → a (mol)
3Fe + 8HNO3 → 3Fe(NO3)2 + 2NO + 4H2O (2)
B → 8/3b → b →2/3b (mol)
TH1: xảy ra phản ứng (1) tạo muối Fe(NO3)3 => nFe(NO3)3 = nNO = 0,03 (mol)
=> mmuối = mFe(NO3)3 = 0,03. 242 = 7,26 (g) # 7,82 => loại
TH2: xảy ra phản ứng (2) tạo muối Fe(NO3)2 => nFe(NO3)2 = 3/2 nNO = 3/2 . 0,03 = 0,045 (mol)
=> mmuối = mFe(NO3)2 = 0,045. 180 = 8,1 (g) # 7,82 => loại
TH3: xảy ra cả (1) và (2) phản ứng tạo 2 muối.
Gọi số mol của Fe ở phản ứng (1) và (2) lần lượt là a và b (mol)
Đặt vào phương trình ta có:
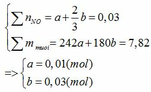
∑ nFe = 0,01 + 0,03 = 0,04 (mol) => mFe = 0,04.56 = 2,24 (g)
∑ nHNO3 pư = 4a + 8/3b = 4. 0,01 + 8/3. 0,03 = 0,12 (mol)
mHNO3 = 0,12.63 = 7,56 (g)
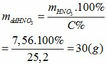
Khối lượng dd sau: mdd sau = mFe + mddHNO3 - mNO = 2,24 + 30 – 0,03.30 = 31,34 (g)
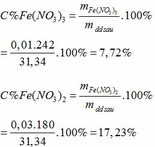

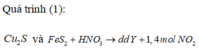
Vì thế Cu và Y vẫn có NO thoát ra
→ chứng tỏ H N O 3 dư
→ chứng tỏ phản úng oxi hóa – khử (1) xảy ra hoàn toàn.
→ khối lượng 12,8 kết hợp bảo toàn electron:
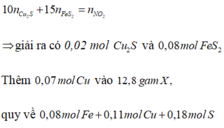
Phản ứng
a m o l H N O 3 → m u ố i F e 2 + ; C u 2 + ; S O 4 2 - ; N O 3 - + 1 , 4 m o l N O 2 + ? m o l N O

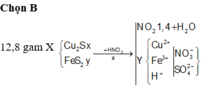
Đáp án là B

Đáp án B
Theo giả thiết và áp dụng bảo toàn electron cho phản ứng của X với HNO3, ta có :
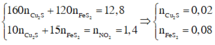
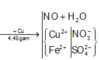
Dung dịch Y gồm Fe3+, Cu2+, SO 4 2 - , NO 3 - , H+. Khi cho Cu (tối đa) vào Y, Cu bị oxi hóa bởi (H+, NO 3 - ) và Fe3+. Vậy bản chất của bài toán là: Hỗn hợp Cu2S, FeS2 và Cu tác dụng với dung dịch HNO3, giải phóng hỗn hợp khí NO, NO2 và tạo ra dung dịch Z. Dung dịch Z có các ion Fe2+, Cu2+, SO 4 2 - , ion còn lại là H+ hoặc NO 3 - . Vì
![]()
nên ion còn lại trong dung dịch Z là ion âm để cân bằng điện tích, đó là ion NO 3 - .
Áp dụng bảo toàn electron và bảo toàn điện tích trong dung dịch Z và bảo toàn nguyên tố N, ta có :