Hỗn hợp X gồm Fe(NO3)2,Cu(NO3)2 và AgNO3 .Thành phần phần trăm khối lượng nitơ trong X là 11,864%. Có thể điều chế tối đa bao nhiêu gam hỗn hợp 3 kim loại từ 14,16 gam X.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án D
% N O 3 - = 11,864:14.62 = 52.54% => % Kim loại = 47,46%
=> mkim loại = 14,16.0,4746 = 6,72 gam.

Đáp án B
Trong 14,16 gam X chứa mN = 14,16 × 0,11864 = 1,68 gam Û nN = 0,12 mol.
Nhận thấy Hỗn hợp X chứa kim loại và gốc nitrat (NO3–).
Từ NO3 ⇒ tỉ lệ nN:nO = 1:3 ⇒ nO = 0,12×3 = 0,36 mol.
Bảo toàn khối lượng hỗn hợp X ⇒ mKim loại = 14,16 – 1,68 – 0,36×16 = 6,72 gam.
⇒ Có thể điều chế tối 6,72 gam hỗn hợp ba kim loại từ 14,16 gam X

Trong 14,16 gam X chứa mN = 14,16 × 0,11864 = 1,68 gam
nN = 0,12 mol.
Nhận thấy Hỗn hợp X chứa kim loại và gốc nitrat (NO3–).
Từ NO3 ⇒ tỉ lệ nN:nO = 1:3
⇒ nO = 0,12×3 = 0,36 mol.
Bảo toàn khối lượng hỗn hợp X
⇒ mKim loại = 14,16 – 1,68 – 0,36×16 = 6,72 gam.
⇒ Có thể điều chế tối 6,72 gam hỗn hợp ba kim loại từ 14,16 gam X
Đáp án B

Đáp án B
Coi hỗn hợp X gồm hỗn hợp kim loại M và gốc NO3
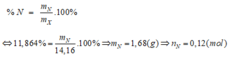
=> nNO3 = nN = 0,12 (mol)
=> m hh M = mX – mNO3 = 14,16 – 0,12. 62 = 6,72 (g)

Đáp án D
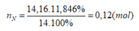
![]()
![]()
Vậy có thể điều chế được tối đa 6,72 gam hỗn hợp kim loại

TBR:
MN=14,16⋅11,864%≈1,68(gam)14,16⋅11,864%≈1,68(gam)
=> nN=1,68:14=0,12(mol)
=> nNO3=nN=0,12(mol)nNO3=nN=0,12(mol)
=> mkim loại=mX−mNO3mX−mNO3=14,16-0,12.62=6,72(gam)
Vậy......

TBR:
MN=\(14,16\cdot11,864\%\approx1,68\left(gam\right)\)
=> nN=1,68:14=0,12(mol)
=> \(n_{NO_3}=n_N=0,12\left(mol\right)\)
=> mkim loại=\(m_X-m_{NO_3}\)=14,16-0,12.62=6,72(gam)
Vậy......

TBR:
MN=14,16⋅11,864%≈1,68(gam)14,16⋅11,864%≈1,68(gam)
=> nN=1,68:14=0,12(mol)
=> nNO3=nN=0,12(mol)nNO3=nN=0,12(mol)
=> mkim loại=mX−mNO3mX−mNO3=14,16-0,12.62=6,72(gam)
Vậy......