Cho 4.48 gam oxit của 1 kim loại hóa trị II tác dụng vừa đủ với 100ml dd H2SO4 0.8M rồi cô cạn dd thì nhận được 13.76g tinh thể muối ngậm nước . Tìm công thức oxit và công thức muối ngậm nước này . (Muối ngậm nước là phân tử muối có kèm theo một số phân tử nươca kết tinh )
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Hướng dẫn giải:
RO + H2SO4 → RSO4 + H2O
0,04 ←0,04
→ Oxit: FeO (72)
CTPT muối ngậm nước là: RSO4.nH2O
n = 0,04 và m = 7,52
=> M = 188
=> n = 2
=> FeSO4 . 2H2O
Vậy CTPT muối ngậm nước là: FeSO4.2H2O

nH2SO4 = 0.04 mol
RO + H2SO4 --> RSO4 + H2O
0.04___0.04
M = 2.88/0.04 = 72
<=> R + 16 = 72
=> R = 56
CTHH: FeO
nFeSO4 = 0.04 mol
M = 7.52/0.04 = 188
<=> 152 + 18n = 188
=> n = 2
CT: FeSO4.2H2O
a) Gọi CTHH là MO
PTHH: MO + H2SO4 ---> RSO4 + H2O
n\(H_2SO_4\) = 0,4 . 0,1 = 0,04 mol
Theo PTHH: nMO = 0,04 mol
MRO = \(\frac{2,88}{0,04}\) <=> R + 16 = 72 <=> R = 56
=> R là Fe
CTHH là FeO
b) Gọi CTHH là FeSO4.xH2O
Theo PTHH: n\(FeSO_4\) = 0,04 mol
M\(FeSO_4\).x\(H_2O\) = \(\frac{7,52}{0,04}\) = 188
<=>( 56 + 32 + 64) + 18x = 188
<=> x = 2
Vậy: CTHH là FeSO4.2H2O

Gọi KL cần tìm là R
\(PTHH:RO+H_2SO_4\rightarrow RSO_4+H_2\)
________MR____98____MR+96_____ 2
_______4,48___7,84____________
\(n_{H2SO4}=0,8.0,1=0,08\left(mol\right)\)
\(\Rightarrow m_{H2SO4}=0,08.98=7,84\left(g\right)\)
Theo PTHH ta có:
\(\frac{4,48}{M_R+16}=\frac{7,84}{98}\)
\(\Rightarrow M_R=4a\left(Ca\right)\)
Kim loại R là Canxi
Nên CTPT của muối ngậm nc:
\(n_{CaSO4}=n_{CaSO4}.xH_2O=0,08\left(mol\right)\)
\(\Rightarrow M_{FeSO4}.xH_2O=\frac{13,76}{0,08}=172\left(\frac{g}{mol}\right)\)
\(\Rightarrow136+18x=172\)
\(\Rightarrow x=2\)
Vậy CTHH cần tìm là CaSO4.2H2O

a)Gọi CTHH của oxit là $RO$
$ RO + H_2SO_4 \to RSO_4 + H_2O$
Theo PTHH : $n_{RO} = n_{H_2SO_4} = 0,1.0,8 = 0,08(mol)$
$\Rightarrow M_{RO} = R + 16 = \dfrac{4,48}{0,08} = 56$
$\Rightarrow R = 40(Canxi)$
b) Gọi CTHH muối ngậm nước là $CaSO_4.nH_2O$
$n_{CaSO_4.nH_2O} = n_{CaSO_4} = n_{H_2SO_4} = 0,08(mol)$
$\Rightarrow M_{CaSO_4.nH_2O} = 152 + 18n = \dfrac{13,7}{0,08} = 171,25$
$\Rightarrow$ Sai đề

\(n_{H_2SO_4}\) = \(\frac{100.24,5\%}{98}\) = 0,25 (mol)
Gọi CTHH của oxit kim loại hóa trị ll là MO
MO + H2SO4 \(\rightarrow\) MSO4 + H2O
0,25<--- 0,25 ---> 0,25 (mol)
MMO = \(\frac{20}{0,25}\) = 80 (g/mol)
\(\Rightarrow\) M = 80 - 16 = 64 (g/mol)
\(\Rightarrow\) M = 64 đvC (Cu : đồng)
\(\Rightarrow\) CuO
Gọi CTHH của tinh thể là CuSO4 . nH2O
ntinh thể = nCuSO4 = 0,25 (mol)
M tinh thể = \(\frac{62,5}{0,25}\) = 250 (g/mol)
\(\Rightarrow\) 160 + 18n = 250
\(\Rightarrow\) n =5
\(\Rightarrow\) CTHH của tinh thể là CuSO4.5H2O
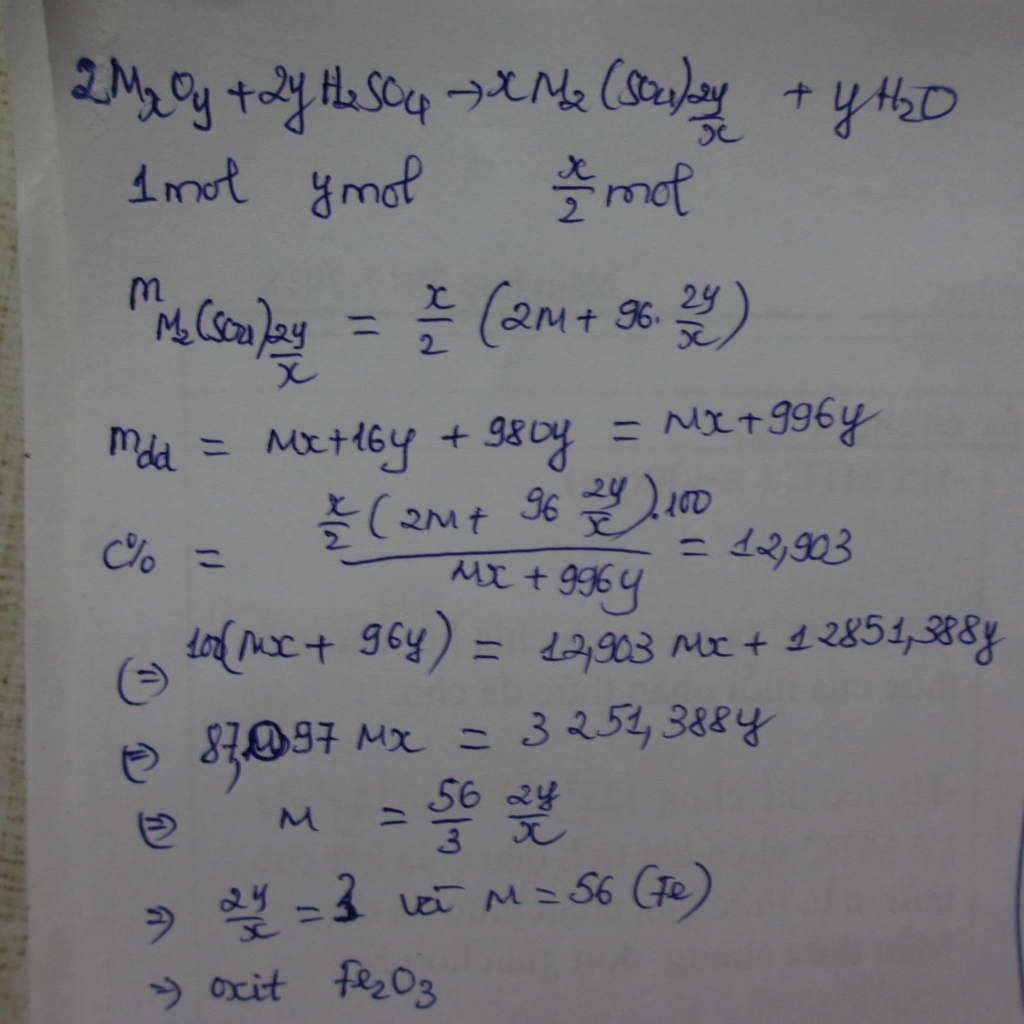

Gọi CTTQ của oxit: MO
nH2SO4 = 0,08 mol
Pt: MO + H2SO4 --> MSO4 + H2O
.....0,08<--0,08-------> 0,08................(mol)
Ta có: 0,08.(M + 16) = 4,48
=> M = 40
=> M là Canxi (Ca)
=> CTPT oxit: CaO
Gọi CTTQ muối ngậm nước: CaSO4.nH2O
ntinh thể = nCaSO4 = 0,08 mol
Ta có: 0,08.(136 + 18n) = 13,76
=> n = 2
=> CTPT muối ngậm nước: CaSO4.2H2O