2. Viết kí hiệu nguyên tửtrong các trường hợp sau:
a.Nguyên tử X ( có7 electron, 7 proton, 7 nơtron).
b.Nguyên tử Y (16 nơtron, 14 electron).
c.Nguyên tử R có 8p và 10 n X có số khối 27, 14n.
d.X có số khối là 20, số p bằng số n.
e.X có điện tích hạt nhân là 13+, có 14 n.
f.X có tổng số hạt là 52, số khối là 35.


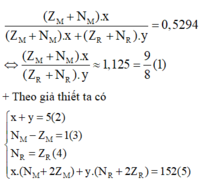
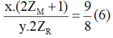
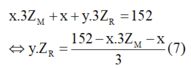
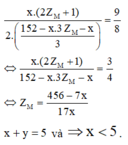
Bài 2:
\(a.Z=P=E=7\\ A=Z+N=7+7=14\left(đ.v.C\right)\\ \Rightarrow KH:^{14}_7N\\ b.Z=P=E=14\\ A=Z+N=14+16=30\left(đ.v.C\right)\\ \Rightarrow KH:^{30}_{14}Si\\ c.Z=P=E=8\\ A=Z+N=8+10=18\left(đ.v.C\right)\\ \Rightarrow KH:^{18}_8O\\ Nguyên.tử.X:\\ Z=P=E=A-N=27-14=13\\ \Rightarrow KH:^{27}_{13}Al\\ d.A=20\left(đ.v.C\right);P=N=\dfrac{A}{2}=\dfrac{20}{2}=10\\ \Rightarrow KH:^{20}_{10}Ne\\ e.Z^+=13^+\Rightarrow Z=13\\ A=Z+N=13+14=27\left(đ.v.C\right)\\ \Rightarrow KH:^{27}_{13}Al\)
\(f.\\ \left\{{}\begin{matrix}P=E\\A=P+N=35\\S=P+N+E=52\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}2P+N=52\\P+N=35\end{matrix}\right.\\ \Leftrightarrow\left\{{}\begin{matrix}P=E=Z=17\\N=18\end{matrix}\right.\\ \Rightarrow A=Z+N=17+18=35\left(đ.v.C\right)\\ \Rightarrow KH:^{35}_{17}Cl\)