Dung dịch A chưa Na+ ( o,1 ) mol , Mg2+ (0,05 ) mol , \(SO_4^{2-}\)(0,04) mol còn lại là Cl- . tính khối lượng muối trong dung dịch
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Giải thích:
BTĐT: 2nMg2++2nCa2+ = nCl- + 2nSO42- + nHCO3- - nNa+
=> 2nMg2+ + 2nCa2+ = 0,01 + 2.0,02 + 0,04 – 0,05 = 0,04 mol
Ta thấy 2(nMg2+ + nCa2+) = nHCO3- => Khi đun nóng mẫu nước trên bị mất tính cứng
Vậy mẫu nước trên là mẫu nước cứng tạm thời
Chú ý:
Nếu mẫu nước đun lên vẫn còn tính cứng thì là nước cứng toàn phần.
Đáp án B

Chọn D
Bảo toàn điện tích: 2.0,05 + 2.0,15 = 0,2 + y → y = 0,2 mol
Đun nóng Y:
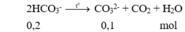
Khối lượng muối khan: 0,05.137 + 0,15.24 + 0,2.35,5 + 0,1.60 = 23,55 gam.

Đáp án C
Bảo toàn điện tích : nHCO3- + nCl- = 2nCa2+ + nNa+ + 2nMg2+
=> nHCO3- = 0,6 mol
2HCO3- -> CO32- + CO2 + H2O
0,6 -> 0,3 mol
Cô cạn dung dịch thu được muối khan gồm (Ca2+ ; Na+ ; Mg2+ ; Cl- ; CO32-)
=> mmuối khan = 75,2g
=>C

Theo ĐLBT ĐT, có: a + 0,15 = 0,1 + 0,15.2 + 0,05.2
⇒ a = 0,35 (mol)
Ta có: mm = mNa + mK + mHCO3- + mCO32- + mSO42-
= 0,35.23 + 0,15.39 + 0,1.61 + 0,15.60 + 0,05.96
= 33,8 (g)
Bạn tham khảo nhé!

Theo định luật bảo toàn điện tích có:

Nên tổng khối lượng kết tủa thu được lớn nhất gồm 0,02 mol Mg(OH)2, 0,01 mol Al(OH)3 và 0,02 mol BaSO4
Đáp án B

Câu 3 :
\(pH=-log\left[H^+\right]=-log\left(0.1\right)=1\)
Câu 4 :
Chứa các ion : H+ , Cl-
Câu 5 :
\(n_{NaOH}=n_{HCl}=0.02\cdot0.1=0.002\left(mol\right)\)
\(\Rightarrow x=\dfrac{0.002}{0.01}=0.2\left(M\right)\)
Câu 1 :
Bảo toàn điện tích :
\(n_{SO_4^{2-}}=\dfrac{0.2\cdot2+0.1-0.05}{2}=0.225\left(mol\right)\)
\(m_{Muối}=0.2\cdot64+0.1\cdot39+0.05\cdot35.5+0.225\cdot96=40.075\left(g\right)\)
Câu 2 :
\(\left[Na^+\right]=\dfrac{0.15\cdot0.5\cdot2+0.05\cdot1}{0.15+0.05}=1\left(M\right)\)
Gọi x là sô mol của ion Cl-
0,1.1+0,05.2=0,04.2+x.1
=> x = 0,12
mmuối=0,1.23+0,05.24+0,04.96+0,12.35,5=11,6(g)