cho a gam hỗn hợp A gồm Na và Fe vào một lượng H2O dư,Sau khi phản ứng xảy ra hoàn toàn người ta thu được 3,36 lit khí (đktc)và chât rắn không tan B. Lọc lấy chất ranwss B, cho vào dung dịch HCl dư, Thấy xuất hiện 4,48 lít khi (đktc),
a. Hãy giải thích các hiện tượng xảy ra ? Viết PTHH
b. Tính %m mỗi chất trong hỗn hợp A?

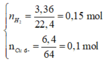
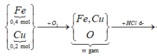
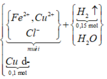

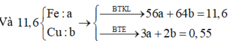
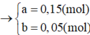

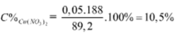


a)
$2Na + 2H_2O \to 2NaOH + H_2$
Natri tan dần, lăn tròn trên mặt nước, có khí không màu không mùi thoát ra. Chất rắn không tan B là Fe
$Fe + 2HCl \to FeCl_2 + H_2$
Sắt tan dần, có bọt khí không màu không mùi bay lên
b)
Thí nghiệm 1, $n_{H_2} = \dfrac{3,36}{22,4} = 0,15(mol)$
$n_{Na} = 2n_{H_2} = 0,3(mol)$
Thí nghiệm 2, $n_{H_2} = \dfrac{4,48}{22,4} = 0,2(mol)$
$n_{Fe} = n_{H_2} = 0,2(mol)$
Suy ra :
$\%m_{Na} = \dfrac{0,3.23}{0,3.23 + 0,2.56}.100\% = 38,12\%$
$\%m_{Fe} = 100\% - 38,12\% = 61,88\%$
ranwss cái này là rắn nhé
Sorry các bạn