Viết các phương trình hóa học xảy ra, tính khối lượng dung dịch sau phản ứng, thể tích dung dịch sau phản ứng và số mol chất tan sau phản ứng :
1. Cho P2O5 vào dd H3PO4
2. Cho P2O5 vào dd KOH
3. Sục SO2 vào dd Na2SO3
4. Sục khí SO2 vào dd Ca(OH)2
5. Sục SO2 vào dd KOH
6. Cho Ba vào dd H2SO4. Tính thể tích H2
7. Cho BaO vào dd H2SO4
8. Cho mẩu Na vào dd CuSO4
9. Cho SO3 vào dd HCl
10. Cho P2O5 vào dd CuCl2
11. Cho Na2O vào dd NaOH
12. Cho SO2 vào dd H2SO4
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a. PTHH: Zn + H2SO4 ---> ZnSO4 + H2↑
b. Ta có: \(C_{M_{H_2SO_4}}=\dfrac{n_{H_2SO_4}}{200:1000}=1,5M\)
=> \(n_{H_2SO_4}=0,3\left(mol\right)\)
Ta lại có: \(n_{Zn}=\dfrac{16,25}{65}=0,25\left(mol\right)\)
Ta thấy: \(\dfrac{0,3}{1}>\dfrac{0,25}{1}\)
Vậy H2SO4 dư.
Theo PT: \(n_{H_2}=n_{Zn}=0,25\left(mol\right)\)
=> \(V_{H_2}=0,25.22,4=5,6\left(lít\right)\)
c. Theo PT: \(n_{ZnSO_4}=n_{Zn}=0,25\left(mol\right)\)
=> \(m_{ZnSO_4}=0,25.161=40,25\left(g\right)\)
d. Ta có: \(V_{dd_{ZnSO_4}}=0,2\left(lít\right)\)
=> \(C_{M_{ZnSO_4}}=\dfrac{0,25}{0,2}=1,25M\)

trên mạng mk thấy có một bài tượng tự trên hocmai, bạn vào đó tham khảo nhé
Nhưng mà bài đó không phải là tính số mol mà tính nồng độ phần trăm mình xem bài đó rồi bạn

a/ \(n_{KOH}=0,2.1=0,2\left(mol\right);n_{H_2SO_4}=0,3.1=0,3\left(mol\right)\)
PTHH: 2KOH + H2SO4 → K2SO4 + 2H2O
Mol: 0,2 0,1 0,1
Ta có: \(\dfrac{0,2}{2}< \dfrac{0,3}{1}\) ⇒ KOH hết, H2SO4 dư
b/ \(m_{H_2SO_4dư}=\left(0,3-0,1\right).98=19,6\left(g\right)\)
c/ Vdd sau pứ = 0,2 + 0,3 = 0,5 (l)
d/ \(C_{M_{ddK_2SO_4}}=\dfrac{0,1}{0,5}=0,2M\)
\(C_{M_{ddH_2SO_4dư}}=\dfrac{0,3-0,1}{0,5}=0,4M\)

a. Các phản ứng có thể xảy ra :
P2O5 + 3H2O -> 2H3PO4
KOH + H3PO4 -> KH2PO4 + H2O
2KOH + H3PO4 -> K2HPO4 + 2H2O
3KOH + H3PO4 -> K3PO4 + 3H2O
b.Gọi nP2O5 = x mol
=> nH3PO4(X) = 0,01+ 2x (mol)
, nKOH = 0,1 mol
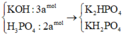
+) TH1 : Nếu KOH dư => chất rắn gồm : (0,01 + 2x) mol K3PO4 ; (0,07 – 6x) mol KOH
=> 6,48 = 212(0,01 + 2x) + 56(0,07 – 6x) => x = 0,005 mol => m = 0,71g
=> 6,48g X gồm : 4,24g K3PO4 và 2,24g KOH
+) TH2 : Nếu chất rắn gồm : (0,08 – 2x) mol K3PO4 ; (4x – 0,07) mol K2HPO4
, mK3PO4 < 6,48g => 0,08 – 2x < 0,03 => x > 0,025
=> 6,48 = 212(0,08 - 2x) + 174(4x – 0,07) => x = 0,00625 mol (L)
+) TH3 : Nếu chất rắn gồm : (0,09 - 2x) mol K2HPO4 ; (4x – 0,08) mol KH2PO4
,mK2HPO4 < 6,48g => 0,09 – 2x < 0,037 => x > 0,043
=> 6,48 = 174(0,09 - 2x) + 136(4x – 0,08) => x = 0,0086 mol (L)
+) TH4 : Nếu H3PO4 dư => nKH2PO4 = 0,1 mol => mKH2PO4 = 13,6g > 6,48g (L)

\(n_{Zn}=\dfrac{6.5}{65}=0.1\left(mol\right)\)
\(n_{H_2SO_4}=0.3\cdot1=0.3\left(mol\right)\)
\(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
\(0.1........0.1...........0.1.......0.1\)
\(\Rightarrow H_2SO_4dư\)
\(n_{H_2SO_4\left(dư\right)}=0.3-0.1=0.2\left(mol\right)\)
\(n_{ZnSO_4}=n_{H_2}=0.1\left(mol\right)\)
\(C_{M_{ZnSO_4}}=\dfrac{0.1}{0.3}=0.33\left(M\right)\)
\(C_{M_{H_2SO_4\left(dư\right)}}=\dfrac{0.2}{0.3}=0.66\left(M\right)\)
\(a) Zn + H_2SO_4 \to ZnSO_4 + H_2\\ b) n_{Zn} = \dfrac{6,5}{65} = 0,1 < n_{H_2SO_4} =0,3 \to H_2SO_4\ dư\\ n_{H_2SO_4\ pư} = n_{ZnSO_4} = n_{Zn} = 0,1(mol)\\ n_{H_2SO_4\ dư} = 0,3 - 0,1 = 0,2(mol)\\ c) C_{M_{ZnSO_4}} = \dfrac{0,1}{0,3} = 0,33M\\ C_{M_{H_2SO_4}} = \dfrac{0,2}{0,3} = 0,67M\)

Câu 2:
1/ - Na: Na tan, có khí thoát ra, giấy quỳ chuyển xanh.
PT: \(Na+2H_2O\rightarrow2NaOH+H_2\)
- Cu: không tan
- CaO: tan, tỏa nhiệt, giấy quỳ chuyển xanh.
PT: \(CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
- SO2: tan, giấy quỳ chuyển đỏ.
PT: \(SO_2+H_2O⇌H_2SO_3\)
- P2O5: tan, giấy quỳ chuyển đỏ.
PT: \(P_2O_5+3H_2O\rightarrow2H_3PO_4\)
- MgO: không tan.
2/ - Trích mẫu thử.
- Hòa tan từng mẫu thử vào nước có quỳ tím.
+ Không tan: CaCO3.
+ Tan, quỳ tím chuyển đỏ: P2O5.
PT: \(P_2O_5+3H_2O\rightarrow2H_3PO_4\)
+ Tan, có khí thoát ra, quỳ tím chuyển xanh: Na
PT: \(2Na+2H_2O\rightarrow2NaOH+H_2\)
+ Tan, quỳ tím chuyển xanh: Na2O.
PT: \(Na_2O+H_2O\rightarrow2NaOH\)
+ Tan, quỳ tím không đổi màu: NaCl.
- Dán nhãn.

1) Gọi số mol P2O5 là a (mol)
PTHH: P2O5 + 3H2O --> 2H3PO4
a----------------->2a
\(m_{H_3PO_4\left(tổng\right)}=98.2a+\dfrac{10.200}{100}=196a+20\left(g\right)\)
mdd sau pư = 142a + 200 (g)
=> \(C\%_{dd.sau.pư}=\dfrac{196a+20}{142a+200}.100\%=17,93\%\)
=> a = 0,093 (mol)
=> mP2O5 = 0,093.142 = 13,206 (g)
2)
a) \(n_{O_2}=\dfrac{10,08}{22,4}=0,45\left(mol\right)\)
PTHH: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
0,9<-----------0,45<----0,45<----0,45
=> \(m_{KMnO_4\left(Pư\right)}=0,9.158=142,2\left(g\right)\)
=> \(m_{KMnO_4\left(tt\right)}=\dfrac{142,2.100}{80}=177,75\left(g\right)\)
=> \(m=\dfrac{177,75.100}{90}=197,5\left(g\right)\)
b)
X \(\left\{{}\begin{matrix}m_{K_2MnO_4}=0,45.197=88,65\left(g\right)\\m_{MnO_2}=0,45.87=39,15\left(g\right)\\m_{KMnO_4}=177,75-142,2=35,55\left(g\right)\\m_{tạp.chất}=197,5.10\%=19,75\left(g\right)\end{matrix}\right.\)