Cho 39,4g hỗn hợp gồm kcl và kClO3, thêm vào đó 0,6g MnO2 làmxúc tác, đun nóng hỗn howpjkhi phản ứng xảy ra hoàn toàn thu được chất rắn có khối lượng 30,4g.Hãy xác định % khối lượng mỗi muối trong hỗn hợp đầu
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


mgiảm = mO2 (sinh ra) = 200 + 3 - 145,4 = 57,6 (g)
\(\rightarrow n_{O_2}=\dfrac{57,6}{32}=1,8\left(mol\right)\)
PTHH: 2KClO3 --to, MnO2--> 2KCl + 3O2
1,2 1,8
\(\rightarrow m_{KClO_3}=1,2.122,5=147\left(g\right)\\ \rightarrow\left\{{}\begin{matrix}\%m_{KClO_3}=\dfrac{147}{200}=73,5\%\\\%m_{KCl}=100\%-73,5\%=26,5\%\end{matrix}\right.\)
Khối lượng oxi thoát ra: 197 + 3 – 152 = 48(g)
Số mol O2=4832=1,5(mol)O2=4832=1,5(mol)
Phương trình hóa học của phản ứng :
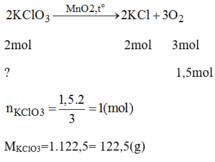
2KClO3MnO2,to⟶2KCl+3O22KClO3⟶MnO2,to2KCl+3O2
2 mol 3 mol
1,5×23=1mol1,5×23=1mol ←← 1,5 mol
Khối lượng KClO3KClO3 trong hỗn hợp : 1 x 122,5 =122,5 (g)Khối lượng KCl trong hỗn hợp ban đầu: 197 – 122,5 = 74,5(g)→%mKClO3=62,18%;%mKCl=37,82%→%mKClO3=62,18%;%mKCl=37,82%

Khối lượng oxi thoát ra: m O 2 = 197 + 3 – 152 = 48(g)
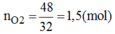
PTHH của phản ứng:
Khối lượng của KCl trong hỗn hợp ban đầu:
m K C l = 197-122,5 = 74,5(g)
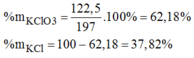

Đáp án A.
Bảo toàn khối lượng: mO2 = 3 + 197 – 152 = 48 (gam)
nO2 = 1,5 (mol)
2KClO3 → 2KCl + 3O2 ↑
⇒ mKCl = 197 – 1.122,5 = 74,5 (gam)

KMnO4-----to----> K2MnO4 + MnO2 + O2
2 KClO3 -----to-----> 2 KCl + 3O2
Rắn B gồm K2MnO4 + MnO2 và KCl
Khi cho B vào dd H2SO4 khí tạo thành là khí Cl2 và số mol Cl2 = 0,015 mol
Vì bảo toàn số nguyên tử Cl => số mol KCl = 0,03
Khối lượng KCl = 0,03.74,5 = 2,235
khối lượng hỗn hợp A = 2,235.100/75,62 = 2,956 gam
P/ư:
2H2SO4 +2 KCl + MnO2 -----> K2SO4 + MnSO4 + Cl2 +2 H2O
4H2SO4 +4 KCl + K2MnO4 -----> 3K2SO4 + MnSO4 + 2Cl2 +4 H2O
Đây bạn nhé !!

Do khối lượng chất rắn trong X và Y bằng nhau
=> Lượng O2 sinh ra khi phân hủy KClO3 phản ứng hết với Cu
PTHH: 2KClO3 --to--> 2KCl + 3O2
a--------------->1,5a
2Cu + O2 --to--> 2CuO
3a<--1,5a
=> b \(\ge\) 3a