13. Khi phân tích định lượng một hợp chất của rượu (X) có thành phần là: 52,17%C, 13,04%H, 34,79%O. Biết 1 lít khí (X) (Đktc) nặng 2,07g. Công thức phân tử của X là:
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án A
Thành phần % khối lượng của O = 100 – (52,17 + 13,04) = 34,79%
nC : nH : nO = 52,17/12 : 13,04 : 34,79/16 = 4,35 : 13,04 : 2,17 = 2: 6: 1
=> Công thức đơn giản nhất là C 2 H 6 O 2 .
M = (2x12+6+16)n = 46 => n =1
Vậy công thức phân tử: C 2 H 6 O 2

\(M_A=23.2=46(g/mol)\)
Trong 1 mol A: \(\begin{cases} n_C=\dfrac{46.52,17\%}{12}=2(mol)\\ n_H=\dfrac{46.13,04\%}{1}=6(mol)\\ n_O=\dfrac{46.34,79\%}{16}=1(mol) \end{cases}\)
Vậy \(CTHH_A:C_2H_6O\)

\(Đặt:CTHH:C_xH_yO_z\)
\(x:y:z=\dfrac{52.17}{12}:\dfrac{13.04}{1}:\dfrac{34.78}{16}=4.3475:13.04:2.17375=2:6:1\)
\(CTđơngiản:\left(C_2H_6O\right)_n\)
\(M_Y=\dfrac{9.2}{\dfrac{5.6}{28}}=46\left(\dfrac{g}{mol}\right)\)
\(\Leftrightarrow46n=46\\ \Leftrightarrow n=1\)
\(Vậy:CTHH:C_2H_6O\)
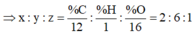


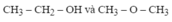
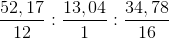
Ta có :
\(M_X=\dfrac{2,07}{\dfrac{1}{22,4}}=46\)(g/mol)
Gọi CTPT của X là $C_xH_yO_z$
Ta có :
\(\dfrac{12x}{52,17}=\dfrac{y}{13,04}=\dfrac{16z}{34,79}=\dfrac{46}{100}\)
Suy ra: x = 2 ; y = 6 ; z = 1
Vậy CTPT là $C_2H_6O$