một hỗn hợp X gồm 0.04 mol Al và 0.06 mol Mg. nếu đem hỗn hợp X hòa tan hoàn toàn trong HNO3 đặc nóng thu được 0.03 mol sản phẩm Y do sự khử của \(N^{+5}\). Nếu đem hỗn hợp X đó hòa tan trong H2SO4 đặc nóng thì thu được 0.12mol sản phẩm Z do sự khử của \(S^{+6}\).Y và Z lần lượt là
A.N2O , H2S
B.NO2, SO2
C.NO2 , SO2
D.NH4NO3 , H2S

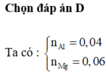
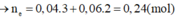
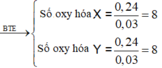


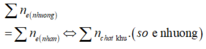
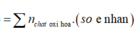
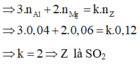
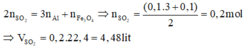
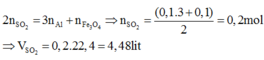
vì Al, Mg đều là những kim loại hóa trị không đỏi nên khi tác dụng với HNO3 và H2SO4 đều lên mức OXH giống nhau vậy số e nhường là như nhau
Al ➝ Al+3 + 3e Mg ➝ Mg+2 + 2e
0,04 → 0,12 0,06→ 0,12
tổng số mol e nhường = 0,12+ 0,12 = 0,24 mol
N+5 + ne → N5-n
0,24→ 0,24/n
⇒ 0,24/n = 0,03 ⇒ n=8
⇒X là N2O hoặc NH4NO3
S+6 + me ➙ S6-m
0,24→ 0,24/m
⇒0,24/m = 0,12 ⇒ m=2 ⇒ Y là SO2