Cho 13.32g kim loại kìm tác dụng với H2O thu được khí A. Cho khí này đi qua bột CuO nung nóng thu được 61.44g kim loại Cu. Xác định kim loại kìm
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án B
Ta có n H 2 = P V R T = 1 . 6 , 11 22 , 4 273 ( 273 + 25 ) = 0 , 25 m o l
Gọi A là kí hiệu, nguyên tử khối của kim loại.
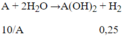
⇒10/A= 0,24 →A = 40 (Ca)

\(n_{H_2}=\dfrac{1,344}{22,4}=0,06\left(mol\right)\) \(n_{H_2SO_4}=0,3.0,25=0,075\left(mol\right)\)
\(X+H_2SO_{4\left(l\right)}\rightarrow XSO_4+H_2\uparrow\)
0,06 0,06 0,06 0,06 (mol)
dư:0 0,015 0 0 (mol)
b/
m\(M_X=\dfrac{3,36}{0,06}=56\left(g\right)\)
\(\rightarrow Fe\)
c/
\(2Fe+6H_2SO_{4\left(đn\right)}\rightarrow Fe_2\left(SO_4\right)_3+3SO_2+6H_2O\)
0,06 0,09 (mol)
V\(_{SO_2}=0,09.22,4=2,016\left(l\right)\)

1.
RCO3 -> RO + CO2
Áp dụng ĐLBTKL ta có:
mRCO3=mRO+mCO2
=>mCO2=10-5,6=4,4((g)\(\Leftrightarrow\)0,1(mol)
VCO2=22,4.0,1=2,24(lít)
Theo PTHH ta có:
nRCO3=nCO2=0,1(mol)
MRCO3=\(\dfrac{10}{0,1}=100\)
=>MR=100-60=40
=>R là Ca
4.
R + H2SO4 -> RSO4 + H2
nH2=0,5(mol)
Theo PTHH ta có:
nR=nH2=0,5(mol)
MR=\(\dfrac{12}{0,5}=24\)
=>R là Mg

1.
2M + 2xHCl \(\rightarrow\)2MClx + xH2
nH2=\(\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Theo PTHH ta có:
nM=\(\dfrac{2}{x}\)nH2=\(\dfrac{0,6}{x}\)
MM=\(\dfrac{5,4}{\dfrac{0,6}{x}}=9x\)
Với x=3 thì MM=27
Vậy M là Al

a) PTHH: X + 2HCl ----> XCl2 + H2\(\uparrow\)
n\(H_2\) = \(\dfrac{0,6}{2}=0,3\left(mol\right)\)
Theo PTHH: nHCl = 2n\(H_2\) = 2.0,3 = 0,6 (mol)
=> mHCl = 0,6. 36,5 = 21,9 (g)
b) Theo PTHH: nX = n\(H_2\) = 0,3 (mol)
=> MX = \(\dfrac{19,5}{0,3}=65\) (g/mol)
=> X là Zn

Gọi hóa trị của M là : n (n∈{1; 2;3})
PTHH:
2M+ 2nHCl→ 2MCln+ nH2↑
Ta có pt:\(\frac{10,8}{M}\text{.( M+ 35,5n)= 53,4}\)
⇒ n= 3; M=27
Vậy M là Nhôm (Al)
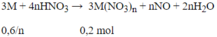
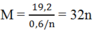
Gọi CT của kim loại kìm đó là M
2M+2H2O->2MOH+H2
H2+CuO->Cu+H2O
nCu=61,44/64=0,96(mol)
=>nH2=0,96(mol)
=>nM=0,96/2=1,92(mol)
MM=\(\dfrac{13,32}{1,92}=7\)
=> kim loại đó là Liti (Li)