Cho 13,2 gam hỗn hợp gồm hai kim loại cùng hoá trị vào 400 ml dd HCl , 1,5 M cô cạn dung dịch thì thu được 32,7 gam hỗn hợp muối khan .
a, Chứng minh hỗn hợp A không tan hết .
b, Tính thể tích H2 ở điều kiện tiêu chuẩn.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

CHÚC BẠN HỌC TỐT!![]()
Gọi M,N lần lượt là hai kim loại có cùng hóa trị trong hh A và x là hóa trị của hai kim loại.
PTHH: \(2M+2xHCl\rightarrow2ACl_x+xH_2\)
PTHH: \(2N+2xHCl\rightarrow2NCl_x+xH_2\)
a) \(n_{HCl}=0,4.1,5=0,6\left(mol\right)\)
\(n_{Cl\left(tạomuối\right)}=0,6\left(mol\right)\)
\(m_{Cl\left(tạomuối\right)}=0,6.35,5=31,3\left(g\right)\)
Ta có: \(m_{muốiclorua}=m_{kloại}-m_{Cl\left(tạomuối\right)}\)
\(m_{kloại}=32,7-21,3=11,4\left(g\right)\)
Vì \(11,4< m_{hhX}\) nên hỗn hợp kim loại không tan hết.
b) \(n_{H2}=\dfrac{n_{HCl}}{2}=\dfrac{0,6}{2}=0,3\left(mol\right)\)
\(\Rightarrow V_{H2}=22,4.0,3=6,72\left(l\right)\left(đktc\right)\)
Vậy.............
Bạn bị sai chỗ
Mkl =32,7-21,3=11,4
Phải là mkl =32,7-31,3=1,4 nha

Giả sử A tác dụng vừa đủ với 400 ml dd HCl 1,5M
nHCl=0,6(mol)
Ta có;
nCl=nHCl=0,6(mol)
mmuối tạo ra=13,2+35,5.0,6=34,5(g)
mà theo giả thiết thu dc 32,7g muối nên A chưa tan hết

a) \(n_{H_2}=\dfrac{3,024}{22,4}=0,135\left(mol\right)\)
=> nHCl = 0,27 (mol)
Theo ĐLBTKL: mkim loại + mHCl = mmuối + mH2
=> mmuối = 5,85 + 0,27.36,5 - 0,135.2 = 15,435 (g)
b) VH2 = 3,024 (l) (Theo đề bài)
c)
Hỗn hợp kim loại gồm \(\left\{{}\begin{matrix}Al:a\left(mol\right)\\X:3a\left(mol\right)\end{matrix}\right.\)
=> 27a + MX.3a = 5,85
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
a----------------------->1,5a
X + 2HCl --> XCl2 + H2
3a------------------->3a
=> 1,5a + 3a = 0,135
=> a = 0,03 (mol)
=> MX = 56 (g/mol)
=> X là Fe

\(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
=> nHCl = 0,8 (mol)
Theo ĐLBTKL: mA,B + mHCl = mmuối + mH2
=> mA,B = 39,4 + 0,4.2 - 0,8.36,5 = 11 (g)

a)
$R + 2HCl \to RCl_2 + H_2$
$2B + 6HCl \to 2BCl_3 + 3H_2$
$n_{H_2} = \dfrac{5,6}{22,4} = 0,25(mol)$
$n_{HCl} = 2n_{H_2} = 0,5(mol)$
Bảo toàn khối lượng : $m_{muối} = m_{kl} + m_{HCl} - m_{H_2}$
$= 9,2 + 0,5.36,5 - 0,25.2 = 26,95(gam)$
b) $V_{dd\ HCl} = \dfrac{0,5}{2} = 0,25(lít)$

Đáp án A
Tại catot có thể lần lượt xảy ra các quá trình:
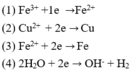
Tại anot có thể lần lượt xảy ra các quá trình:
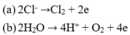
Sau khi điện phân A, cho dung dịch này phản ứng với NaOH thu được kết tủa B, nung B đến khối lượng không đổi thu được hỗn hợp 2 oxit. Trong A có 2 loại ion kim loại
Mặt khác, khi điện phân dung dịch A cho đến khi hết ion Cl - thì catot tăng 6,4 gam
⇒ Quá trình (2) đã xảy ra một phần, Cu 2 + vẫn còn trong dung dịch sau điện phân.
Gọi số mol Fe 3 + , Cu 2 + , Cl - , SO 4 2 - trong 100ml dung dịch A lần lượt là a,b,c,d.
Khi điện phân hết 
Theo bảo toàn e: số e do Fe3+ và Cu2+ nhận bằng số mol Cl- nhường. a + 0,1.2 = c (1)
Khối lượng dung dịch giảm gồm Cu2+ và Cl- đã phản ứng và bị tách ra khỏi dung dịch
6,4 + 35,5c = 17,05 (2)
Sau khi điện phân A, cho dung dịch này phản ứng với NaOH thu được kết tủa B, nung B đến khối lượng không đổi được 16 gam 2 oxit
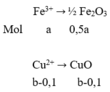
Suy ra: 160,0,5a + 80(b – 0,1) = 16 (3)
Theo định luật bảo toàn điện tích, đối với dung dịch A ta có:
3a + 2b = c + 2d (4)
Giải hệ phương trình ta được:
a = 0,1; b = 0,2; c= 0,3; d = 0,2
Khối lượng muối trong 100ml dung dịch A là 48,25 gam

m m u ố i = m K L + m C l -
⇒ m C l = m m u o i - m K L
= 23,85 - 13,2 = 10,65g
⇒ n C l - = 10,65/35,5 = 0,3 mol
⇒ n H 2 = 1/2 nCl- = 0,15 mol
⇒ V = 0,15.22,4 = 3,36 lit
⇒ Chọn B.

a) nHCl = 0,8.0,35 = 0,28 (mol)
mmuối = mKL + mCl = 3,64 + 0,28.35,5 = 13,58 (g)
b)
3,64 gam X phản ứng vừa đủ với 0,28 mol HCl
=> 3,64 gam X phản ứng vừa đủ với 0,28 mol H+
=> 1,82 gam X phản ứng vừa đủ với 0,14 mol H+
=> 1,82 gam X phản ứng vừa đủ với \(\dfrac{0,14}{2}=0,07\) mol H2SO4
mH2SO4 = 0,07.98 = 6,86 (g)
Cần thêm C% để tính m dung dịch nhé :)
mCl trong muối = 32,7 - 13,2 = 19,5g => nCl = 19,5 ; 35,5 \(\approx0,55\)
Mà nHCl = 0,4. 1,5 = 0,6 > 0,55
=> HCl dư