Câu 1: (1,0 điểm)Hòa tan hoàn toàn 42,6 gam hỗn hợp X gồm một kim loại kiềm và một kim loại kiềm thổ có tỉ lệ mol tương ứng là 5:4 vào 500 ml dung dịch HCl 1M thu được dung dịch Y và 17,472 lít khí (đktc)
a. Xác định thành phần % về khối lượng mỗi kim loại trong X.
b. Dẫn từ từ khí CO2 vào dung dịch Y, tính thể tích khí CO2 (đktc) cần dùng để thu được lượng kết tủa lớn nhất
Câu 9 : (1,0 điểm)Hòa tan hoàn toàn một lượng AlCl3 và một lượng Al2(SO4)3 vào nước thu được 200 gam dung dịch X, chia dung dịch X thành hai phần:
- Phần 1: cho tác dụng với BaCl2 dư thu được 13,98 gam kết tủa trắng.
- Phần 2: cho tác dụng với 476 ml dung dịch Ba(OH)2 1M, sau khi phản ứng xong thu được 69,024 gam kết tủa. Biết khối lượng phần 2 gấp n lần khối lượng phần 1 (n là số nguyên dương) và lượng chất tan trong phần 2 nhiều hơn lượng chất tantrong phần 1 là 32,535gam. Tính nồng độ phần trăm của các chất có trong dung dịch X
Câu 3: (1,0 điểm)Tiến hành thí nghiệm sau:
- Thí nghiệm 1: cho 1,74 gam MnO2 tác dụng với HCl đặc, dư, đun nóng thu được khí A màu vàng lục.
- Thí nghiệm 2: cho một lượng sắt vào dung dịch H2SO4 loãng đến khi khối lượng dung dịch tăng 167,4 gam thì thu được một lượng khí B.
- Thí nghiệm 3: thêm 3 gam MnO2 vào 197 gam hỗn hợp KCl và KClO3 thu được hỗn hợp X. Trộn kĩ và đun nóng hỗn hợp X đến khi phản ứng xảy ra hoàn toàn thì thu được chất rắn nặng 152 gam và một lượng khí D.
- Thí nghiệm 4: Nạp toàn bộ lượng khí A, khí B và khí D thu được ở các thí nghiệm trên vào một bình kín, nâng nhiệt độ cao để thực hiện hoàn toàn các phản ứng rồi đưa nhiệt độ về 25ºC thu được dung dịch Y chỉ chứa một chất tan duy nhất. Viết các phương trình hóa học xảy ra và tính nồng độ % của chất tan có trong dung dịch Y.


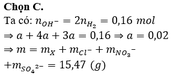

Câu 3: M giải qua rồi nên t giải tắt cho lẹ :D
Thích để phân số thì t làm phân số vậy (:
\(MnO_2\left(0,02\right)+4HCl\left(đăc\right)\rightarrow MnCl_2+Cl_2\left(0,02\right)+4H_2O\)
nMnO2 = 0,02 (MOL) => nCl2 = 0,02 (mol)
\(Fe\left(a\right)+H_2SO_4\rightarrow FeSO_4+H_2\left(a\right)\)
Gọi a là số mol Fe phản ứng
Theo đề => \(56a-2a=167,4\)
\(\Rightarrow a=3,1\left(mol\right)\)=> nH2 = 3,1 (mol)
Đun nóng hoàn toàn X thì:
\(2KClO_3-t^o->2KCl+3O_2\)
=> Chất rắn còn lại là MnO2 và KCl không bị nhiệt phân
Ta có: \(\left\{{}\begin{matrix}m_{MnO_2}=3\\m_{KCl}+m_{KClO_3}=197\\m_{MnO2}+m_{KCl}=152\end{matrix}\right.\)\(\Rightarrow\left\{{}\begin{matrix}m_{MnO_2}=3\left(g\right)\\m_{KCl}=149\left(g\right)\\m_{KClO_3}=48\left(g\right)\end{matrix}\right.\)
\(\Rightarrow n_{KClO_3}=\dfrac{96}{245}\left(mol\right)\)
=> \(n_{O_2}=\dfrac{144}{245}\left(mol\right)\)
* Thí nghiệm 4:
\(O_2\left(\dfrac{144}{245}\right)+2H_2\left(\dfrac{288}{245}\right)-t^o->2H_2O\left(\dfrac{288}{245}\right)\)
\(H_2\left(0,02\right)+Cl_2\left(0,02\right)-t^o->2HCl\left(0,04\right)\)
Dung dịch Y: HCl
=> nHCl = 0,04 (mol) => mHCl = 1,46 (g)
nH2O = \(\dfrac{288}{245}\) (mol) => mH2O = \(\dfrac{5184}{245}\) (g)
\(\Rightarrow C\%_{HCl}=\dfrac{1,46.100}{\dfrac{5184}{245}+1,46}=6,45\%\)
Câu 1:
A, B lần lượt là kim loại kiềm, kiềm thổ
\(2A\left(a\right)+2HCl\rightarrow2ACl+H_2\left(0,5a\right)\)\(\left(1\right)\)
\(B\left(b\right)+2HCl\rightarrow BCl_2+H_2\left(b\right)\)\(\left(2\right)\)
\(n_{HCl}=0,5\left(mol\right)\)
\(n_{H_2}=0,78\left(mol\right)\)
Gỉa sử lượng HCl tham gia phản nứng hết
=> nH2 = 1/2nHCl = 0,25 (mol) < 0,78 (mol)
=> A, B còn dư tác dụng với nước có trong dung dịch HCl
\(2A\left(1,25x-a\right)+2H_2O\rightarrow2AOH+H_2\left(0,625x-0,5a\right)\)\(\left(3\right)\)
\(B\left(x-b\right)+2H_2O\rightarrow B\left(OH\right)_2+H_2\left(x-b\right)\)\(\left(4\right)\)
Ta có: \(nA:nB=5:4\)
Gọi x là số mol của B => nA = 1,25x (mol)
\(\Rightarrow1,25xA+xB=42,6\left(I\right)\)
Gọi a, b lần lượt là số mol của A, B ở pt (1) và (2)
Ta có: \(\sum n_{H_2}=0,78=0,5a+b+0,625x+x\)
\(\Leftrightarrow x=0,48\left(mol\right)\)
Thay vào (I) \(\Leftrightarrow0,6A+0,48B=42,6\)
- Vói A = 7 (Li) => B = 80 (loại)
- Với A = 23 (Na) => B = 60 (loại)
- Với A = 39 (K) => B = 40 (Ca) thoã mãn
- A = 85 (Rb) = > B = -17,5 (loại)
- A = 133 (Cs) => B = -77,5 (loại)
- A = 223 (Fr) = > B = -290 (loại)
Vậy A: K,
B: Ca