cho 6.32g chất rắn CuO, MxOy(M là kim loại có nhiều hóa trị)+CO dư(pư hoàn toàn) được h2 khí C, h2 chất rắn D(D gồm 2 kim loại nguyên chất). Dẫn C vào KOH đặc dư thì bình KOH tăng 3,96g. Cho cả D+dd H2SO4 loãng dư được dd E và chất rắn G ko tan. Cho G+AgNO3 đủ được 10,8gAg(các pư hoàn toàn). Tìm MxOy, % m các chất 2 oxit ban đầu
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
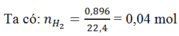
Gọi: nNa = x mol ⇒ nAl = 2x mol
Phản ứng:
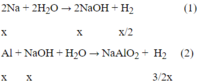
Sau các phản ứng còn m(g) chất rắn không tan, đó là khối lượng của Al dư.
Theo phản ứng (1), (2)
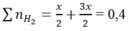
![]()
⇒mAl ban đầu = 2x = 0,2.2 = 0,4 mol
Mà: nAl phản ứng = nNaOH = x = 0,2 mol ⇒ nAl dư = 0,4 - 0,2 = 0,2 mol
⇒mAl = 0,2.27 = 5,4 (g)

Đáp án C
Ta có: nH2= 0,04 mol
Gọi: nNa = x mol " nAl = 2x mol
Phản ứng:
2Na + 2H2O → 2NaOH + H2 (1)
x x x 2
Al + NaOH + H2O → NaAlO2 + 3 2 H2 (2)
x x 3 2 x
Sau các phản ứng còn m(g) chất rắn không tan, đó là khối lượng của Al dư.
Theo phản ứng (1) ; (2)

⇒ mAl ban đầu = 2x = 0,2.2 = 0,4 mol
Mà: nAl phản ứng = nNaOH = x = 0,2 mol ⇒ nAl dư = 0,4 - 0,2 = 0,2 mol
⇒ mAl = 0,2.27 = 5,4 (g)

Đáp án B
Các phương trình hóa học:
MxOy + yCO → xM + yCO2
Ca(OH)2 + CO2 → CaCO3 + H2O
Ta có: moxit = mkim loại + moxi
Trong đó:
![]()
→moxit = 2,5 + 0,15.16 = 4,9 gam

Gọi X là kim loại hóa trị II.
nHCl = 0,35 (mol)
X + 2HCl → XCl2 + H2
nX = 11,7/X (mol)
Vì sau khi phản ứng, chất rắn không tan hết
=> 11,7/X > 0,35/2
=> X < 67 (lấy xấp xỉ thôi) (*)
Vì nếu thêm 50ml dung dịch HCl thì chất rắn tan, dung dịch tác dụng với CaCO3 tạo CO2 => HCl còn dư
VddHCl = 400ml => nHCl = 0,4 (mol)
=> 11,7/X < 0,4/2 => X > 56 (*) (*)
Từ (*) và (*) (*) ta có khoảng của X:
56 < X < 67
Mà X là kim loại hóa trị II, tác dụng được với HCl
=> X là: Zn

Đáp án C
Gọi a, b là số mol CuO và FexOy, viết sơ đồ phản ứng ta có:
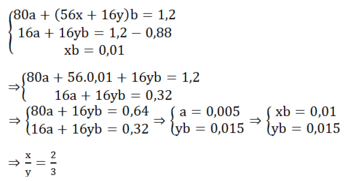





\(CuO\left(0,05\right)+CO-t^o->Cu\left(0,05\right)+CO_2\left(0,05\right)\)\(\left(1\right)\)
\(M_xO_y\left(\dfrac{0,04}{y}\right)+yCO-t^o->xM+yCO_2\left(0,04\right)\)\(\left(2\right)\)
Hỗn hợp C:\(\left\{{}\begin{matrix}CO_2\\CO\left(dư\right)\end{matrix}\right.\)
Hỗn hợp chất rắn D:\(\left\{{}\begin{matrix}Cu\\M\end{matrix}\right.\)
Khi Dẫn C vào KOH đặc dư thì chỉ có CO2 tác dụng
\(CO_2+2KOH--->K_2CO_3+H_2O\)\(\left(3\right)\)
Sau phản ứng thấy khối lượng bình tăng thêm 3,96 gam chính là khối lượng CO2 bị hấp thụ vào bình
\(n_{CO_2}=\dfrac{3,96}{44}=0,09\left(mol\right)\)
Khi cho D tác dụng với H2SO4 loãng dư thì thu dduwwocj chất rắn G không tan và đung dịch E sau phản ứng. Chứng tỏ kim loại M tán trong dung dịch H2SO4 loãng dư:
\(2M+nH_2SO_4\left(loang\right)--->M_2\left(SO_4\right)_n+nH_2\)\(\left(4\right)\)
Dung dịch E là: \(M_2\left(SO_4\right)_n\)
Chất rắn G là: \(Cu\)
Khi cho G tác dụng với lượng vừa đủ AgNO3 thì:
\(Cu+2AgNO_3--->Cu\left(NO_3\right)_2+2Ag\)\(\left(5\right)\)
\(n _{Ag}=\dfrac{10,8}{108}=0,1\left(mol\right)\)
Theo (5) \(n_{Cu}=0,05\left(mol\right)\)
Theo (1) \(n_{CuO}=0,05\left(mol\right)\)
\(\Rightarrow m_{CuO}=4\left(g\right)\)
\(\Rightarrow m_{M_xO_y}=6,32-4=2,32\left(g\right)\)
Theo (1) \(n_{CO_2}\left(1\right)=0,05\left(mol\right)\)
\(\Rightarrow n_{CO_2}\left(2\right)=0,04\left(mol\right)\)
\(\Rightarrow n_{M_xO_y}=\dfrac{0,04}{y}\left(mol\right)\)
Ta có: \(\dfrac{0,04}{y}=\dfrac{2,32}{Mx+16y}\)
\(\Leftrightarrow M=\dfrac{1,68y}{0,04x}\)
\(\Rightarrow CT:Fe_3O_4\)
\(\%m_{Cu}=63,29\%\)
\(\%m_{Fe_3O_4}=36,71\%\)
cảm ơn bạn nhé