Hãy tìm công thức hóa học đơn giản nhất của một loại oxit của lưu huỳnh, biết rằng trong oxit này có 2 g lưu huỳnh kết hợp với 3 g oxi.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(\frac{n_S}{n_O}=\frac{\frac{2}{32}}{\frac{3}{16}}=\frac{1}{3}\Rightarrow SO_3\)
Giả sử CTHH là SxOy , ta có tỉ lệ:
\(\dfrac{x}{y}\)=\(\dfrac{2}{32}\):\(\dfrac{3}{16}\)=\(\dfrac{1}{3}\)⇒CTHH là SO3

Số mol của nguyên tử lưu huỳnh là: 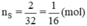
Số mol của nguyên tử oxi là: 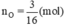
Ta có: 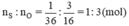
⇒ Trong một phân tử lưu huỳnh trioxit có 1 nguyên tử S và có 3 nguyên tử O.
Vậy công thức hóa học đơn giản nhất của oxit lưu huỳnh là SO3.

Gọi công thức của oxit là SxOy.
PTHH: \(2xS+yO_2\underrightarrow{t^o}2S_xO_y\)
Ta có: nS = 2/32 = 0,0625 mol; nO2 = 3/32 = 0,09375
\(\Rightarrow\dfrac{x}{y}=\dfrac{n_S}{2n_{O2}}=\dfrac{0,0625}{0,1875}=\dfrac{1}{3}\)
Công thức của oxit là SO3.

Gọi công thức là SxOy (x,y \(\in\) N*)
x : y = \(\dfrac{2}{32}:\dfrac{3}{16}\)
= 0,0625 : 0,1875
= 1 : 3
\(\rightarrow\) x = 1, y = 3
Vậy công thức là SO3
Gọi CTHH dạng chung là SxOy
Ta có x:y=\(\dfrac{2}{32}:\dfrac{3}{16}=1:3\)
=>x=1;y=3
Vậy CTHH:SO3
Chúc bạn học tốt![]()

\(m_S=\dfrac{64.50}{100}=32\left(g\right)=>n_S=\dfrac{32}{32}=1\left(mol\right)\)
\(m_O=\dfrac{64.50}{100}=32\left(g\right)=>n_O=\dfrac{32}{16}=2\left(mol\right)\)
=> CTHH: SO2

Ta có: \(\left\{{}\begin{matrix}m_S=64\cdot50\%=32\left(g\right)\\m_O=64\cdot50\%=32\left(g\right)\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}n_S=\dfrac{32}{32}=1\left(mol\right)\\n_O=\dfrac{32}{16}=2\left(mol\right)\end{matrix}\right.\)
Vậy CTHH là \(SO_2\)
Số mol của nguyên tử lưu huỳnh là: nS =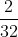 (mol)
(mol)
Số mol của nguyên tử oxi là: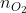 =
= 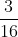 mol
mol
Ta có: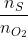 =
= 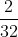 :
: 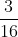 =
= 
Vậy công thức hóa học đơn giản nhất của oxit lưu huỳnh là SO3
Số mol của nguyên tử lưu huỳnh là: nS =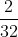 (mol)
(mol)
Số mol của nguyên tử oxi là: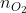 =
= 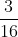 mol
mol
Ta có: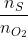 =
= 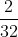 :
: 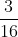 =
= 
Vậy công thức hóa học đơn giản nhất của oxit lưu huỳnh là SO3