tìm x,y trong công thức xCuSO4*yH2O. Biết trong phân tử muối ngậm nước này CuSO4 chiếm 47,05% về khối lượng
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


ta có. \(\frac{106}{\left(106+18\right).x}.100\%=37,07\Rightarrow x\approx2\)

Gọi công thức muối ngậm nước có dạng: RSO 4 . nH 2 O
Theo đề bài ta có hệ phương trình:
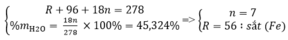
Vậy công thức của muối sắt là: FeSO 4 . 7 H 2 O

Gọi công thức phân tử ngậm nước là: \(RSO_4.nH_2O\)
Đề bài quá mơ hồ . Phiền em xem lại đề bài rồi

a) Gọi CTHH của muối A là NaxSyOz
%mO = 100% - 32,39% - 22,54% = 45,07%
Ta có x : y : z = \(\frac{32,39\%}{23}\) : \(\frac{22,54\%}{32}\) : \(\frac{45,07\%}{16}\)
= 1,4 : 0,7 : 2,8
= 2 : 1 : 4
\(\Rightarrow\) CTHH của A : Na2SO4
b) CTHH của B là Na2SO4 . aH2O
%mmuối = \(\frac{142}{142+18a}\) . 100%=55,9%
Giải pt ta đc: a = 6
=> Na2SO4 . 6H2O

gọi CTHH của A là NaxSyOz ta có 23x:32y:16z=32,29:22,54:45,07
=0,14:0,07:0,28
=2:1:4
-> CTHH :Na2SO4
b)Gọi CTHH của B là Na2SO4.nH2O
Ta có 142.100/142+18n=55,9%
->14200=55,9(142+18n)
->n=6
-> CTHH Na2SO4.6H2O
c) ta có nNa2SO4.6H2O=0,1.1=0,1(mol)
-> mNa2SO4.6H2O=250.0,1=25(g)

a) \(\%Mg=\dfrac{24}{24+2.M_X+18n}.100\%=11,82\%\)
=> MX + 9n = 89,523
Xét n = 5 => MX = 44,5 (Loại)
Xét n = 6 => MX = 35,5 => X là Cl
Xét n = 7 => MX = 26,5 (Loại)
Xét n = 8 => MX = 17,5 (loại)
Vậy CTHH của tinh thể là MgCl2.6H2O
b) \(\%Cl=\dfrac{35,5.2}{203}.100\%=34,975\%\)
c) \(n_{MgCl_2.6H_2O}=\dfrac{40,6}{203}=0,02\left(mol\right)\)
=> nH = 0,02.12 = 0,24 (mol)
=> \(n_{H_3PO_4}=\dfrac{0,24}{3}=0,08\left(mol\right)\)
=> mH3PO4 = 0,08.98 = 7,84 (g)