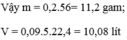Nung 5,6g sắt với S dư trong bình kín không có không khí. Phản ứng xong đem hòa tan sản phẩm trong dung dịch HCL 3,65% vừa đủ thấy dùng hết m gam dung dịch HCl Tính m gam
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


- Chất rắn không tan trong HCL dư là S => m S dư = 3,8g
Kết tủa đen là CuS => n CuS = 0,1 = n H 2 S = nS phản ứng
m S phản ứng = 3,2g
0,2 mol Z gồm 0,1 mol H 2 S và 0,1 mol H 2
m ban đầu = 3,8 + 3,2 = 7g
Ta lại có
n Fe p / u = n S p / u = 0,1 mol
n Fe dư = n H 2 = 0,1 mol
n Fe ban đầu → m Fe ban đầu = 0,2 .56 = 1,12 g
Vậy m = 11,2 + 0,7 = 18,2 (gam)

a)
\(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\); \(n_S=\dfrac{1,6}{32}=0,05\left(mol\right)\)
PTHH: Zn + S --to--> ZnS
Xét tỉ lệ: \(\dfrac{0,1}{1}>\dfrac{0,05}{1}\) => Zn dư, S hết
Các PTHH:
Zn + S --to--> ZnS
ZnS + 2HCl --> ZnCl2 + H2S
Zn + 2HCl --> ZnCl2 + H2
B chứa H2, H2S
b)
PTHH: Zn + S --to--> ZnS
0,05<-0,05-->0,05
ZnS + 2HCl --> ZnCl2 + H2S
0,05-->0,1----->0,05--->0,05
Zn + 2HCl --> ZnCl2 + H2
0,05-->0,1----->0,05-->0,05
=> nHCl = 0,1 + 0,1 = 0,2 (mol)
\(C\%_{dd.HCl}=\dfrac{0,2.36,5}{100}.100\%=7,3\%\)
c) \(\%V_{H_2S}=\%V_{H_2}=\dfrac{0,05}{0,05+0,05}.100\%=50\%\)
d) \(\overline{M}=\dfrac{0,05.2+0,05.34}{0,05+0,05}=18\left(g/mol\right)\)
=> \(d_{B/H_2}=\dfrac{18}{2}=9\)

a)
Fe + S --to--> FeS
Fe + 2HCl --> FeCl2 + H2
FeS + 2HCl --> FeCl2 + H2S
\(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\); \(n_S=\dfrac{4,8}{32}=0,15\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,1}{1}< \dfrac{0,15}{1}\) => Fe hết, S dư
=> Chất sau khi nung gồm FeS, S dư
b)
PTHH: Fe + S --to--> FeS
0,1->0,1------->0,1
FeS + 2HCl --> FeCl2 + H2S
0,1-------------------->0,1
=> Y là H2S
VH2S = 0,1.22,4 = 2,24 (l)
c) Z là S
mS = (0,15 - 0,1).32 = 1,6 (g)

a) \(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
\(n_S=\dfrac{1,6}{32}=0,05\left(mol\right)\)
PTHH: Fe + S --to--> FeS
0,05<-0,05-->0,05
Fe + 2HCl --> FeCl2 + H2
0,05->0,1---->0,05-->0,05
FeS + 2HCl --> FeCl2 + H2S
0,05-->0,1----->0,05--->0,05
=> \(\%V_{H_2S}=\%V_{H_2}=\dfrac{0,05}{0,05+0,05}.100\%=50\%\)
b)
nNaOH = 0,3 (mol)
- Gọi số mol HCl trong B là a (mol)
PTHH: NaOH + HCl --> NaCl + H2O
a<-----a
FeCl2 + 2NaOH --> Fe(OH)2 + 2NaCl
0,1---->0,2
=> a + 0,2 = 0,3
=> a = 0,1 (mol)
\(C_{M\left(FeCl_2\left(B\right)\right)}=\dfrac{0,1}{0,5}=0,2M\)
\(C_{M\left(HCl\left(B\right)\right)}=\dfrac{0,1}{0,5}=0,2M\)
nHCl(bđ) = 0,3 (mol)
=> \(C_{M\left(dd.HCl\left(bđ\right)\right)}=\dfrac{0,3}{0,5}=0,6M\)

Đáp án D
Ta có: n H C l p h ả n ứ n g = 2 n O = 0 , 12 . 2 = 0 , 24 m o l → n H C l d ư = 0 , 06 m o l
Cho AgNO3 dư vào X thu được kết tủa gồm AgCl và Ag.
Bảo toàn Cl:
n A g C l = 0 , 03 . 2 + 0 , 24 + 0 , 06 = 0 , 36 m o l → n A g = 0 , 015 m o l
Cho AgNO3 vào X thì xảy ra quá trình:
4 H + + N O 3 - + 3 e → N O + 2 H 2 O A g + + e → A g
Bảo toàn e toàn quá trình:
n F e = 0 , 06 . 4 + 0 , 03 . 2 + 0 , 06 . 3 4 + 0 , 015 3 = 0 , 12 m o l → m = 6 , 72 g a m

Đáp án D
Ta có
![]()
![]()
Cho AgNO3 dư vào X thu được kết tủa gồm AgCl và Ag.
Bảo toàn Cl: ![]()
![]()
Cho AgNO3 vào X thì xảy ra quá trình:
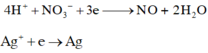
Bảo toàn e toàn quá trình:
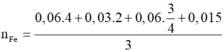
=> m = 6,72 (g)
D vì:
Ta có
Cho AgNO3 dư vào X thu được kết tủa gồm AgCl và Ag.
Bảo toàn Cl:
Cho AgNO3 vào X thì xảy ra quá trình:
Bảo toàn e toàn quá trình:
=> m = 6,72 (g)