Khi đốt nóng 1 g sắt kết hợp với 1,9 g clo tạo ra hợp chất sắt clorua. Biết phân tử của hợp chất chỉ chứa một nguyên tử sắt. Công thức phân tử của hợp chất là? Mọi người giúp mình với ạ, mình đang cần gấp 😢
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Phản ứng xảy ra như sau:
2Mg + xCl2 \(\rightarrow\) 2MgClx
1/24 2,96/71
Ta có: x/24 = 2.2,96/71
x = 2.

bài 1: gọi công thức là CxHy
ta có: %C=81,82%=>%H=100-81,82=18,18%
theo đề ta có x:y=\(\frac{81,82}{12}:\frac{18,18}{1}\)=2:5
vậy công thức là C2H5

2) \(\%m_{\dfrac{O}{FeO}}=\dfrac{16}{72}.100\approx22,222\%\\ \%m_{\dfrac{O}{Fe2O3}}=\dfrac{3.16}{160}.100=30\%\\ \%m_{\dfrac{O}{Fe3O4}}=\dfrac{64}{232}.100\approx27,586\%\)
Bài 1:
%mO=48%
M(phân tử)= (2.56)/28%=400(g/mol)
Số nguyên tử S: (24% . 400)/32= 3(nguyên tử)
Số nguyên tử O: (48% . 400)/16= 12(nguyên tử)
=> CTHH: Fe2(SO4)3

Công thức chung của hợp chất F e x O y .
Theo đề bài ta có:
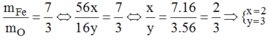
Vậy CTHH của hợp chất là F e 2 O 3 .
Phân tử khối là: 56.2 + 16.3 = 160 (đvC)

- Số mol H2 là: nH2 = 4,48/22,4= 0,2 (mol)
- Số mol H2O là: nH2 = 1,204.10^23/6,02.1023 = 0,2 (mol)
- Gọi CTHH của hợp chất là: FexOy (x,y nguyên dương)
- PTPU: FexOy + yH2 →→ xFe + yH2O (1)
Theo (1) : Số mol H2O = số mol H2
Theo ĐB: số mol H2O = số mol H2 = 0,2 mol
Vậy H2 phản ứng hết và FexOy còn dư
- Theo ĐB: nH2O = 0,2 mol →→ nO = 0,2 mol →→mO = 0,2.16 =3,2(g)
1. m = Y + mO = 14,2 + 3,2 = 17,4 (g)
2. Khối lượng Fe trong Y hay khối lượng của Fe sinh ra ở (1) là: mFe = 14,2.59,155/100 =8,4g
-Từ CTHH của X: FexOy ta có:
x:y = mFe/56: mO/16= 8,4/56: 3,2/16 = 0,15:0,2 = 3:4
Vậy: x = 3, y = 4. CTHH của X: Fe3O4
3. Theo phần trên FexOy dư sau phản ứng ( Fe3O4 dư sau phản ứng) mFexOy dư = mFe3O4 dư = 14,2 – 8,4 = 5,8 (g)

Gọi CTHH của hợp chất là FexCly.
Ta có: 56x + 35,5y = 127
Với x = 1 ⇒ y = 2 → FeCl2.
Với x = 2 ⇒ y = 0,42 (loại)
Với x = 3 ⇒ y = -1,15 (loại)
Vậy: CTHH cần tìm là FeCl2

Khi đun nóng :
1g Mg ................................................2,96g Cl
Vậy
24g Mg ....................................................71g Cl
\(n_{Mg}=\dfrac{24}{24}=1\left(mol\right)\)
\(n_{Cl}=\dfrac{71}{35,5}=2\left(mol\right)\)
Vậy công thức hoá học của hợp chất là \(MgCl_2\)

-Khí clo do nguyên tố clo tạo nên, phân tử gồm 2 nguyên tử clo liên kết nhau.
=> Khí clo là đơn chất, Công thức hóa học là \(Cl_2\), PTK = 35,5 x 2 = 71 (đvC)
-Khí ozon do nguyên tố oxi tạo nên, phân tử gồm 3 nguyên tố oxi liên kết nhau
=> Khí ozon là đơn chất, Công thức hóa học là \(O_3\), PTK = 16 x 3 = 48 (đvC)
- Nhớ tick [Nếu đúng] ha ♥