Ngâm một thanh sắt vào dung dịch chứa 9,6 gam muối sunfat của kim loại hóa trị II, sau khi kết thúc phản ứng thanh sắt tăng thêm 0,48 gam. Vậy công thức hóa học của muối sunfat là:
A. CuSO4
B. CdSO4
C. NiSO4
D. ZnSO4
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Bạn tham khảo nhá!!!
mCuSO4 = = = 32 (gam)
nCuSO4 = = 0,2 (mol)
Gọi x là khối lượng miếng sắt ban đầu.
Khối lượng miếng sắt sau khi nhúng vào dung dịch CuSO4 tăng là:
= 0,08.x (gam)
Fe + CuSO4 ---> FeSO4 + Cu
1mol 1mol 1mol 1mol
0,2mol 0,2mol 0,2mol 0,2mol
Khối lượng sắt phản ứng: 0,2.56 = 11,2 (gam)
Khối lượng Cu sinh ra: 0,2.64 = 12,8 (gam)
Khối lượng miếng sắt tăng lên = mCu sinh ra - mFe phản ứng
=> 0,08.x = 12,8 – 11,2
0,08.x = 1,6 => x = 20 (gam)
Vậy khối lượng miếng sắt ban đầu là 20 gam

Đáp án A
Khối lượng kẽm tăng lên chính bằng chênh lệch giữa khối lượng kẽm tan ra và kim loại X bám vào
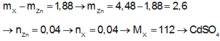

10 ml dung dịch RSO4 cần 0,15.0,02 = 0,003 mol BaCl2
⇒ 50 ml dung dịch RSO4 cần 0,015 mol BaCl2
⇒ R + 96 = 1,8/0,015 ⇒ R = 24 là Mg ⇒ Chọn C.

10 ml dung dịch RSO4 cần 0,003 mol BaCl2
![]() 50 ml dung dịch RSO4 cần 0,015 mol BaCl2
50 ml dung dịch RSO4 cần 0,015 mol BaCl2
![]() RSO4 = 1,8/0,015
RSO4 = 1,8/0,015 ![]() R = 24
R = 24
![]() R là Mg
R là Mg
![]() Chọn C
Chọn C

Chọn C
10 ml dung dịch RSO4 cần 0,15.0,02 = 0,003 mol BaCl2
⇒ 50 ml dung dịch RSO4 cần 0,015 mol BaCl2
R + 96 = 1,8/0,015 R = 24 là Mg
A
giải hẳn ra đc ko bạn