Bài 1: Hòa tan 4,5 gam hợp kim nhôm, magie trong dung dịch H2SO4 loãng, dư, thấy có 5,04 lít khí hiđro bay ra (đktc).
A) Viết phương trình hoá học.
B) Tính thành phần phần trăm khối lượng của các kim loại trong hợp kim.
Bài 2: Cho 5,4 gam Al vào 100 ml dung dịch H2SO4 0.5M.
A) Tính thể tích khí H2 sinh ra (đktc).
B) Tính nồng độ mol của các chất trong dung dịch sau phản ứng. Cho rằng thể tích dung dịch sau phản ứng thay đổi không đáng kể.

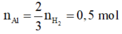
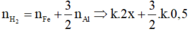
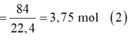
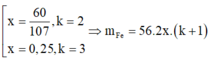
1.nH2=5.04/22.4=0.225mol
Đặt x,y lần lượt là số mol của Al,Mg
a)2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
x 3/2 x
Mg+ H2SO4 --> MgSO4 + H2
y y
b) theo đề, ta có hệ pt: 27x + 24y= 4.5
1.5x + y =0.225
giải hệ pt trên,ta có :x=0.1 ; y=0.075
thay vào pt,suy ra :
mAl=0.1*27=2.7g =>%Al=(2.7/4.5)*100=60%
=>%Mg=40%
vậy % của Al,Mg lần lượt là 60% và 40%
2.nAl=5.4/27=0.2mol
nH2SO4=0.5*0.1=0.05 mol
pt:2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
0.2 0.05 0.02 0.05
a)theo pt, ta thấy Al dư
VH2=0.05*22.4=1.12 l
b)CMAl2(SO4)3= 0.02/0.1=0.2M
Bài này không khó đâu nh,tính theo pthh thôi à.
Chúc em học tốt!!!:))
bạn ơi xem lại đè bài giùm mjk vs ạ