viết phương trình điện ly của những chất sau :
a) Các chất điện ly mạnh : Ba(NO3)2 0,10M , HNO3 0,020M , KOH 0,010M . Tính nồng độ mol của từng ion trong các dung dịch trên .
b) Các chất điện ly yếu : HClO , HNO2
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Các chất điện li mạnh phân li hoàn toàn nên phương trình điện li và nồng độ các ion trong dung dịch như sau:
Ba(NO3)2 → Ba2+ + 2NO-3
0,01M 0,10M 0,20M
HNO3 → H+ + NO-3
0,020M 0,020M 0,020M
KOH → K+ + OH-
0,010M 0,010M 0,010M
b) Các chất điện li yếu phân li không hoàn toàn nên phương trình điện li như sau:
HClO H+ + ClO-
HNO2 H+ + NO-2.

a) Các chất điện li mạnh phân li hoàn toàn nên phương trình điện li và nồng độ các ion trong dung dịch như sau:
Ba(NO3)2 \(\rightarrow\) Ba2+ + 2NO-3
0,01M 0,10M 0,20M
HNO3 \(\rightarrow\) H+ + NO-3
0,020M 0,020M 0,020M
KOH \(\rightarrow\) K+ + OH-
0,010M 0,010M 0,010M
b) Các chất điện li yếu phân li không hoàn toàn nên phương trình điện li như sau:
HClO H+ + ClO-
HNO2 H+ + NO-2.

a, \(Ba\left(NO_3\right)_2\rightarrow Ba^{2+}+2NO_3^-\)
\(HNO_3\rightarrow H^++NO_3^-\)
\(KOH\rightarrow K^++OH^-\)
b, \(HClO⇌H^++ClO^-\)
\(HNO_2⇌H^++NO_2^-\)
\(H_2CO_3⇌2H^++CO_3^{2-}\)

- Chất điện ly mạnh: NaCl; CuSO4; NaOH; Mg(NO3)2; (NH4)3PO4; AgNO3; HNO3.
- Chất điện ly yếu: HF; H3PO4; H2CO3; CH3COOH; Al(OH)3; Fe(OH)2.
- Chất không điện ly: Glucozơ; glyxerol; ancol etylic.
Giải thích các bước giải:
- Chất không điện ly: Glucozơ; glyxerol; ancol etylic.
- Chất điện ly mạnh: NaCl; CuSO4; NaOH; Mg(NO3)2; (NH4)3PO4; AgNO3; HNO3.
Ta có phương trình:
(NH4)3PO4 → 3NH4+ + PO43- AgNO3 → Ag+ + NO3-
NaOH → Na+ + OH- Mg(NO3)2 → Mg2+ + 2NO3-
NaCl → Na+ + Cl- CuSO4 → Cu2+ + SO42-
HNO3 → H+ + NO3-
- Chất điện ly yếu: HF; H3PO4; H2CO3; CH3COOH; Al(OH)3; Fe(OH)2.
Ta có phương trình
Fe(OH)2 ⇔ Fe2+ + OH-
HF ⇔ H+ + F- CH3COOH ⇔ CH3COO- + H+
H3PO4 ⇔ H+ + H2PO4- Al(OH)3 ⇔ Al3+ + 3OH-
HPO42- ⇔ H+ + PO43- HCO3- ⇔ H+ + CO32-
H2PO4- ⇔ H+ + HPO42- H2CO3 ⇔ H+ + HCO3-
- Chất điện ly mạnh: NaCl; CuSO4; NaOH; Mg(NO3)2; (NH4)3PO4; AgNO3; HNO3
\(NaCl\rightarrow Na^++Cl^-\\ CuSO_4\rightarrow Cu^{2+}+SO_4^{2-}\\ NaOH\rightarrow Na^++OH^-\\ Mg\left(NO_3\right)_2\rightarrow Mg^{2+}+2NO_3^-\\ \left(NH_4\right)_3PO_4\rightarrow3NH_4^++PO_4^{3-}\\ AgNO_3\rightarrow Ag^++NO_3^-\\ HNO_3\rightarrow H^++NO_3^-\)
- Chất điện ly yếu: HF; H3PO4; H2CO3; CH3COOH; Al(OH)3; Fe(OH)2
\(HF\rightarrow H^++F^-\\ H_3PO_4\rightarrow H^++H_2PO_4^-\\ H_2PO_4^-\rightarrow H^++HPO_4^{2-}\\ HPO_4^{2-}\rightarrow H^++PO_4^{3-}\\ H_2CO_3\rightarrow H^++HCO_3^-\\ HCO_3^-\rightarrow H^++CO_3^{2-}\)
\(CH_3COOH\rightarrow H^++CH_3COO^-\\ Al\left(OH\right)_3\rightarrow Al^{3+}+3OH^-\\ Fe\left(OH\right)_2\rightarrow Fe^{2+}+2OH^-\)
- Chất không điện ly: Glucozơ; glyxerol; ancol etylic

a)\(BaCl_2\rightarrow Ba^{2+}+2Cl^-\)
0,05 0,05 0,1
\(\left[Ba^{2+}\right]=0,05M\)
\(\left[Cl^-\right]=0,1M\)
b)\(HCl\rightarrow H^++Cl^-\)
0,1 0,1 0,1
\(\left[H^+\right]=0,1M\)
\(\left[Cl^-\right]=0,1M\)

tk
- Chất điện ly mạnh: NaCl; CuSO4; NaOH; Mg(NO3)2; (NH4)3PO4; AgNO3; HNO3.
Phương trình điện ly:
NaCl → Na+ + Cl- CuSO4 → Cu2+ + SO42-
NaOH → Na+ + OH- Mg(NO3)2 → Mg2+ + 2NO3-
(NH4)3PO4 → 3NH4+ + PO43- AgNO3 → Ag+ + NO3-
HNO3 → H+ + NO3-
- Chất điện ly yếu: HF; H3PO4; H2CO3; CH3COOH; Al(OH)3; Fe(OH)2.
Phương trình điện ly:
HF ⇔ H+ + F- CH3COOH ⇔ CH3COO- + H+
H3PO4 ⇔ H+ + H2PO4- Al(OH)3 ⇔ Al3+ + 3OH-
H2PO4- ⇔ H+ + HPO42- H2CO3 ⇔ H+ + HCO3-
HPO42- ⇔ H+ + PO43- HCO3- ⇔ H+ + CO32-
Fe(OH)2 ⇔ Fe2+ + OH-
- Chất không điện ly: Glucozơ; glyxerol; ancol etylic.
a) Các chất điện li mạnh phân li hoàn toàn nên phương trình điện li và nồng độ các ion trong dung dịch như sau:
Ba(NO3)2 → Ba2+ + 2NO-3
0,01M 0,10M 0,20M
HNO3 → H+ + NO-3
0,020M 0,020M 0,020M
KOH → K+ + OH-
0,010M 0,010M 0,010M
b) Các chất điện li yếu phân li không hoàn toàn nên phương trình điện li như sau:
HClO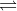 H+ + ClO-
H+ + ClO-
HNO2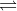 H+ + NO-2.
H+ + NO-2.